Выбор катализатора амидирования и изучение в его присутствии превращения м-толуиловой кислоты в N,N-диэтил-м-толуамид
Продукты реакции анализировали методом ГЖХ на приборе ЛХМ-8МД-5 с пламенно-ионизационным детектором, колонка 3 м х 3 мм, заполнена 15% Апиозона L на хроматоне N-AW-DMCS. Температура хроматографирования от 80 до 240°С с программой 8 К/мин, скорость газа-носителя (азот) 20 см3/мин. Стандартная хроматограмма приведена на рис. 2.1. Воду, содержащуюся в катализате, анализировали на приборе ЛХМ-80 с катарометром, колонка 2 м х 3 мм, заполнена 20% ПЭГ 20М на хроматоне, импрегнированном 2,5% КОН. Температура хроматографирования 150°С, скорость газа-носителя (гелий) 40-45 см3/мин, внутренний стандарт – диметилацетамид. Реакцию амидирования изучали в лабораторном проточном интегральном реакторе стандартной конструкции. Раствор м-толуиловой кислоты в диэтиламине (мольное соотношение 1:1-1:7) насосом-дозатором подавали в верхнюю часть реактора, послойно заполненного кварцевой насадкой и катализатором. Обогрев осуществляли электропечью, контроль температуры проводили в трех точках по высоте слоя катализатора хромелъ-копелевыми термопарами. Охлажденные продукты реакции собирались в ловушке, откуда отбирались на анализ. При обработке оксида алюминия минеральными кислотами выявлено, что катализаторы должны эксплуатироваться сразу после стадии сушки. Предварительная прокалка приводит к потере активности либо до уровня немодифицированного Al2O3, либо снижается в еще более значительной степени. Эксплуатация выбранного гидроксилапатита кальция не требует после стадии приготовления дополнительных активационных обработок. Физико-химические характеристики КФ-70: насыпной вес 0,60 г/см3, прочность 1,0 кг/мм, удельная поверхность 80 м2/г, объем пор 0,65 см3/г, кислотность 5 мг-экв./г; структура - широкопористая (сдвиг кривой распределения пор по эквивалентным радиусам до 150 Å). Активность кальцийфосфатных катализаторов в реакциях кислотного катализа пропорциональна количеству групп HPO42-, содержание которых в исследованном нами образце контакта достигало 30%, что близко к теоретически возможному (33,3%). При необходимости проверки кислотности катализаторов на основе оксидов алюминия порошок контакта суспендировали в ацетонитриле и титровали н-бутиламином, за ходом процесса следили потенциометически. Применение Н0-индикаторов не дает лучших результатов.
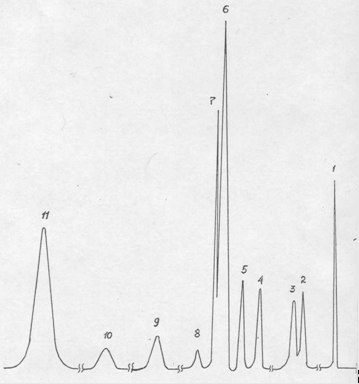
Рис. 2.1. Хроматограмма основных продуктов катализата синтеза м-ДЭТА на катализаторе КФ-70.
1 – диэтиламин, 2,3,8,9,10 – неидентифицированные продукты, 4 – диэтилбензамид, 5- о-ДЭТА, 6 – м-ДЭТА, 11 – тетраэтилизофталамид.
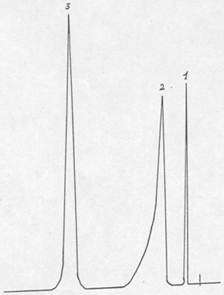
Рис. 2.2. Хроматограмма водных погонов синтеза м-ДЭТА
1 – диэтиламин, 2 – вода, 3 – диэтилацетат (внутренний стандарт)
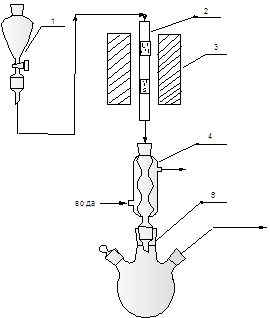
Рис. 2.3. Схема лабораторной установки амидирования в присутствии гетерогенных катализаторов. 1 – бюретка с насос-дозатором, 2 - реактор, 3 – электропечь, 4 - холодильник, 5 – приёмник.
3. Обсуждение результатов. Исследование гетерогенных катализаторов амидирования м-толуиловой кислоты
3.1 Термодинамика процесса
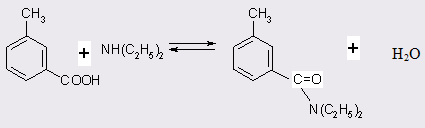
Поскольку реакция амидирования м-толуиловой кислоты (МТК) является обратимой, на первом этапе исследований были изучены термодинамические характеристики процесса. С целью определения состава равновесной смеси и условий, при которых могут быть сняты термодинамические ограничения, на первых порах был проведен расчет констант равновесия при различных температурах в диапазоне 260-320°С для реакции (табл. 3.1).
толуамид катализатор кислота токсикологический
Расчет констант равновесия проводился по экспериментальным данным после достижения в статических условиях устойчивых равновесных концентраций компонент [51]. В качестве катализатора реакции в данном случае использовали 0,5 мас.% хлорной кислоты. Достижение равновесия при любых температурах определялось только с одной стороны (опыты по гидролизу диэтилтолуамида не проводились).
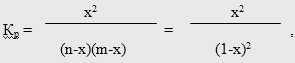
где х - степень превращения МТК или ее мольная доля [52]; n и m - мольные доли исходных компонентов (для простоты принято, что n = m = 1).
Обработка полученных значений Кр по методу наименьших квадратов [53] позволила аппроксимировать их следующим эмпирическим уравнением:
Кр = exp(8,81 – 3019,25/Т),
которое, в частности, может быть использовано при синтезе химико-технологических систем на стадии проектирования.
Расчет термодинамически возможной степени превращения при различных температурах и мольных отношениях реагентов осуществлялся по формуле [51]
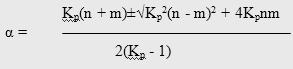
Таблица 3.1 Расчетные значения констант равновесия и термодинамически возможные степени превращения м-толуиловой кислоты при различных условиях синтеза м-ДЭТА
|
t, 0С |
К |
Соотношение МТК:диэтиламин |
Кр |
Степень превращения МТК (α) |
|
260 |
533 |
1:1 1:5 |
21,49 |
0,549 0,880 |
|
280 |
553 |
1:1 1:2 1:5 |
27,96 |
0,840 0,967 0,990 |
|
300 |
573 |
1:1 1:3 1:5 |
36,00 |
0,857 0,986 0,990 |
|
320 |
593 |
1:1 1:2 1:3 1:5 |
40,35 |
0,860 0,970 0,988 0,990 |
Анализ данных, представленных в табл. 3.1, позволяет сделать вывод, что при соотношении МТК: диэтиламин 1:1 мольн. и при 2600С термодинамически возможная степень превращения составляет 0,55, а при 320 0С - 0,86. При температуре 280 0С и мольном соотношении реагентов 1:2 термодинамические ограничения практически снимаются.
Отметим, что небольшие значения констант равновесия свидетельствуют о том, что, несмотря на снятие термодинамических ограничений, реакция по-прежнему остается равновесной. Поэтому дальнейшее увеличение концентрации диэтиламина и повышение температуры максимально благоприятствуют процессу.
Следующей важной характеристикой процесса является тепловой эффект реакции, который из-за отсутствия в литературе термодинамических характеристик исходных и конечных компонент (кроме диэтиламина и воды) был оценен по теплотам сгорания органических соединений в газообразном состоянии, и его величина составила ΔНо298= -20±5 кДж/моль. В свою очередь теплоты сгорания веществ, принимающих участие в реакции, рассчитаны по формуле [54]:
