Выбор катализатора амидирования и изучение в его присутствии превращения м-толуиловой кислоты в N,N-диэтил-м-толуамид
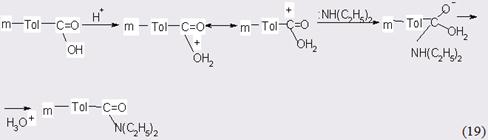
К лимитирующей, по-видимому, следует отнести стадию присоеинения диэтиламина, что не противоречит мнению других исследователей, изучавших аналогичные системы. В силу того, что процесс протекает на гетерогенном катализаторе при достаточно высокой температуре, не исключено, что протонированная молекула м-толуиловой кислоты отщепляет воду с генерацией карбаниона, на который в свою очередь может осуществляться электрофильная атака протонированного амина:
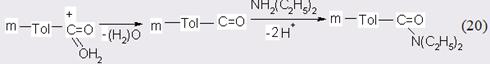
Хотя такой маршрут реакции, возможно, более заманчив, для его реализации требуется участие в переходном состоянии еще одной молекулы диэтиламина, что, как было показано в начале данного раздела, маловероятно. Однако главный с практической точки зрения вывод остается прежним: процесс необходимо катализировать кислотами Бренстеда-Лоури [65]. Во-первых, активность катализатора связана с силой и концентрацией кислоты, во-вторых, увеличение концентрации кислоты может тормозить коксообразовательные процессы и, наконец, в-третьих, имеется возможность найти оптимум между силой кислоты и полезными функциями катализатора.
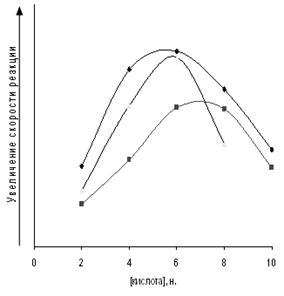
Рис. 3.3. Тенденция изменения скорости реакции амидирования МКТ от концентрации минеральных кислот. 1 − HClO4, 2 − HCl, 3 −HIO3.
Тогда требования к контакту можно сформулировать предельно просто - это должен быть достаточно стабильный катализатор, несущий протонсодержащую функцию. Такие катализаторы, по-видимому, следовало искать среди солеподобных контактов с двух- или трехосновными кислотами.
В заключение рассмотрения теоретических вопросов следует отметить, что поскольку м-толуиловая кислота по условиям ее синтеза содержит орто- и пара-изомеры, а также бензойную кислоту, для выявления реакционной способности всей гаммы продуктов были проведены оценочные опыты на фторированном γ-Al2O3. Полученные результаты сведены в таблицу 3.3.
Таблица 3.3 Относительные скорости амидирования производных бензойной кислоты диэтиламином (мольное отношение реагентов 1:5, t° = 300°С)
|
Положение заместителя в субстрате |
H |
CH3 |
|
Орто |
1 |
0,35 |
|
Мета |
1 |
0,90 |
|
Пара |
1 |
0,85 |
Таким образом, метильная группа в орто-положении стерически препятствует подходу диэтиламина к карбоксильной группе. В свою очередь группа СН3 в мета- и пара-положении в силу эффекта гиперконъюгации тоже тормозит процесс амидирования из-за нагнетания избыточной электронной плотности на атом углерода карбоксильной группы, понижая ее реакционную способность по отношению к диэтиламину. Этот факт вполне согласуется с предложенным выше механизмом и его аутентичностью для водно-кислотных растворов в части участия в процессе карбокатиона. Однако близость относительных скоростей реакций для м- и п-изомеров не исключает возможности генерации карбанионов, о чем говорилось выше.
3.4 Выбор и изучение эффективного катализатора амидирования м-толуиловой кислоты
На основании полученных и представленных выше данных по исследованию катализаторов амидирования МТК, изучению механизм реакции и обнаруженной существенной роли в катализе, в первую очередь, поверхностно закрепленных протонов был проведен поиск контактов, которые в первом приближении могли способствовать решению поставленной задачи.
Поиск такого катализатора осуществлялся целенаправленным путем пропитки нейтрального оксида алюминия неорганическими двух- и трехосновными кислотами с различными значениями pKa = - lgK2 (для H3BO3 – K1, т.к. дальнейшая ионизация затруднена). Количество импрегнируемых кислот расчетно соответствовало одинаковой концентрации атомов водорода (ок. 0,1% на носитель).
Полученные таким образом катализаторы после стандартной обработки испытывали в реакции амидирования МТК при 320°С в течение 1 ч. Обнаружено, что активность контактов связана с силой кислоты (рис. 3.4), т.е. ее способностью диссоциировать; лучшие результаты были достигнуты при использовании о-мышьяковой и о-фосфорной кислот с рКа соответственно 6,98 и 7,21. По-видимому, именно диапазон рКа исходных кислот 6,5-7,5 является оптимальным для решения поставленной задачи. Дополнительные расчеты показывают, что активность катализаторов напрямую не связана с процентной долей атомов водорода в самих кислотах (так, например, [Н] в H3PO4 - 3,1%, в H2TeO3 - 1,1%, в H2SeO3 - 1,6%, в H3BO3 – 4,4%).
Проведенные контрольные опыты по влиянию элементов, входящих в состав кислотных остатков (в этом случае на Al2O3 наносили преимущественно оксиды в количестве до 0,5 мас.% в расчете на соответствующий металл), позволили обнаружить их некоторое катализирующее (B, As, P, Te) или ингибирующее (Mo, Se) действие. Однако при переходе к димолибденовой и селенистой кислотам их каталитический эффект выражен значительно сильнее, чем у нейтрального оксида алюминия.
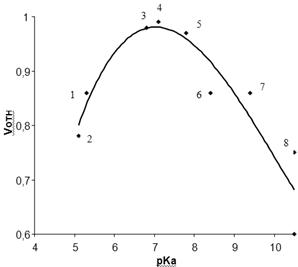
Рис. 3.4. Зависимость относительно скорости амидирования МКТ от величины рКа кислот, нанесенных на нейтральный оксид алюминия (Vотн для Al2O3 ок. 0,45): 1 − H2B4O7, 2 − H2Mo2O7, 3 − H3AsO4, 4 − H3PO4, 5 − H2TeO3, 6 − H2SeO3, 7 − H3BO3, 8 − H2TeO4.
На основании изложенных данных был проведен анализ ряда промышленных катализаторов, что позволило нам выбрать для испытаний системы, применяющиеся для разложения 4,4-диметил-1,3-диоксана в изопрен (производство СКИ). Наибольший интерес представляли марки катализаторов КФ-70, КФ-83 (содержит 0,3 мас.% MnO) и КБФ-76у (дополнительно содержит 0,02 мас.% о-борной кислоты) [66]. Как и следовало ожидать, несколько большую активность (на 3-4%) и особенно селективность (на 8%) проявил гидроксилапатит кальция (КФ-70) общей формулы:
Ca10-х-уHx+y(PO4)6(OH)2-x-y(x+y ≤ 2).
Дальнейшие испытания катализатора были проведены по обычной схеме, а часть результатов представлена в таблице 3.4. Анализ этих данных свидетельствует о том, что оптимальной температурой синтеза м-ДЭТА является 300-320°С, объемной нагрузкой по сырью - 0,2 ч-1. В этих условиях синтеза достигается 85-86%-ный выход целевого продукта. При соотношении МТК: диэтиламин 1:5 при прочих равных условиях выход ДЭТА имеет оптимум (табл. 3.4, 3.5), а конверсия и селективность процесса превышают 90% (92,4 и 94,5, 92,8 и 91,4 соответственно при 300 и 320°С).
Для дополнительной иллюстрации изложенного материала на рис. 3.5 и 3.6 представлены зависимости степени превращения МТК и селективности образования ДЭТА от условного времени контакта при различных температурах. Независимо от температуры, степень превращения МТК достигает максимума при τ 20 г∙мин/моль, однако селективность процесса по истечении этого периода начинает уменьшаться, что вызвано вторичным превращением целевого продукта, в первую очередь, увеличением скорости реакции переаминирования:
