Редкоземельные металлы и их полуторные оксиды
Таблица 10. Различные конфигурации координационной сферы
|
Координационное число |
Конфигурации координа- [ ционной сферы |
Отношение радиусов |
|
3 4 4 6 8 12 |
Треугольник АХ3 Тетраэдр АХ4 Квадрат АХ4 Октаэдр AX6 Куб AX8 Плотнейшая кубическая или гексагональная упаковка АХ12 |
0.158 ≤А ≤ 0.225 0.225 ≤ к ≤ 0.415 0.415 ≤ к ≤ 0.732 0.415 ≤ к ≤ 0.732 0.732 ≤ А ≤1.00 k≈1.0 |
В настоящее время в физике твердого тела приводится следующее объяснение этой таблицы. Взаимодействие сферически симметричных ионов является ненаправленным и ненасыщенным. Ненасыщенность ионной связи проявляется в том, что каждый ион стремится приблизить к себе как можно больше противоположна заряженных ионов, т. е. образовать структуру с возможно более высокими координационными числами. Однако эти конфигурации неустойчивы в том случае, если катионы настолько малы, что свободно помещаются между анионами и могут «болтаться» в соответствующих пустотах. Если катион приблизится к части окружающих его анионов (к. ч. понизится), то электростатическая энергия системы ионов уменьшится, а, следовательно, устойчивость системы возрастет [38].
Структура А-типа (гексагональная) состоит из координационных полиэдров, расположенных вокруг ионов редкоземельного элемента. Каждый полиэдр образован семью ионами кислорода, три из которых расположены на более удаленном расстоянии и четыре – на более близком расстоянии. Например, для La3О3 эти расстояния равны 2.68—2.78 А и 2,28—2.48 А соответственно. При переходе от окиси лантана к оксидам редкоземельных элементов с меньшими ионными радиусами расстояния М . . .О соответственно уменьшаются. Однако если в оксидах от La2O3 до Nd2О3 сумма ионных радиусов металла и кислорода практически равна расстоянию М . . .О, то начиная с Sm303 ![]() < dM…O, что приводит к неустойчивости структуры А-формы для оксидов элементом с ионным радиусом, меньшим, чем у неодима.
< dM…O, что приводит к неустойчивости структуры А-формы для оксидов элементом с ионным радиусом, меньшим, чем у неодима.
В структуре В-формы (моноклинной) имеется три типа координационных полиэдров. Общим для всех трех типов является то, что расстояния М. . .О для шести кислородных ионов несколько меньше, чем в соответствующей А-форме, в то время как седьмой ион значительно удален. Так, для окиси самария среднее значение М. . .О для шести кислородных атомов составляет 2.38—2.41 А, седьмой же кислородный атом находится от атома металла на расстоянии 2.71- 2.76 или 3.12 А в зависимости от типа полиэдра. Это позволяет некоторым авторам рассматривать структуру В-формы как состоящую из смеси МО6- и МО7- полиэдров, а следовательно, являющуюся промежуточной между А- и С-формами, структуры которых создаются из одного типа координационных полиэдров (МО7 — в гексагональном А-типе и МО6 — в кубической С-форме). Структура В-формы является устойчивой для оксидов самария, европия и гадолиния вплоть до температур 2000—2300°.
В кубической С-форме кристаллизуются оксиды редкоземельных элементов, имеющие меньший ионный радиус, чем гадолиний. Так как увеличение температуры равносильно увеличению «эффективного» радиуса катиона, можно наблюдать обратимый фазовый переход для оксидов, находящихся на границе устойчивости С- и В-форм или В- и А- форм. В предыдущих разделах было показано, что для оксидов диспрозия, тербия и гольмия в действительности наблюдается обратимый переход С ↔ В-типа, а для оксидов европия и самария — переход В ↔А-типа, причем чем меньше ионный радиус элемента при стандартных условиях, тем до более высоких температур нужно нагреть оксид, чтобы осуществить превращение С ↔В или В ↔А. В работе Ладда и Ли [39] были рассчитаны энергии решеток оксидов редкоземельных элементов. Расчет проводился с использованием как формулы Борна—Габера
U=ΔH— (I + S)M — ![]() — E0 + 2RT
— E0 + 2RT
где U — энергия решетки, ΔH — энтальпия образования оксида, (I + S)M —энергия ионизации и сублимации редкоземельного металла, ![]() и ЕО — энергия диссоциации и сродство к электрону для кислорода, так и по формуле
и ЕО — энергия диссоциации и сродство к электрону для кислорода, так и по формуле
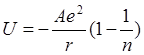
где А — константа Маделунга, г — расстояние между ближайшими ионами противоположного знака, п — степень потенциалf отталкивания. На рис. 46 представлены расчетные данные Лада и Ли для энергии А- и С-форм оксидов в зависимости от ионного радиуса редкоземельного элемента, а также ориентировочный ход кривой энергии решетки для В-формы оксидов.
Наблюдаемые области Стабильности различных структурных форм хорошо согласуются с предположением, что тип полуторной окиси, существующий при обычном давлении, всецело определяется температурой и размером катиона. Тем не менее иногда в процессе образования кристаллического вещества может образоваться структура, энергетически менее выгодная. Но в любом случае реальная кристаллическая решетка будет стабильна при условии абсолютного или относительного минимума свободной энергии. Практически это проявляется в том, что при образовании полуторных оксидов, независимо от размера катиона, сначала образуется С-форма оксида. Для больших катионов эта форма оксида является местабильной, однако переход ее в стабильную равновесную модификацию возможен вплоть до высоких температур.
Относительная устойчивость оксидов в метастабильной С-форме, т.е. оксидов элементов с ионным радиусом, большим, чем у тербия, повышается в ряду от La203 до Gd203. Как видно из рис. 8, одновременно с уменьшением ионного радиуса катиона наблюдается увеличение энергии решетки, а следовательно, и энергии связи М. . .0 [40] (как для устойчивых форм, так и для метастабильной С-формы), что приводит к возрастанию энергии активации и температуры перехода С-формы в устойчивые А- или В-формы.
Кроме этого, уже было показано, что не существует строго определенной температуры фазового перехода, а наблюдается расширенный интервал температур, внутри которого происходит превращение. Так как энергия активации зависит от совершенства кристаллической решетки метастабильной фазы, ширина температурного интервала и его положение сильно зависят от предыстории образца и от дефектности его структуры.
Для обратимых фазовых превращений классическая теория требует наличия определенной температуры перехода кубической модификации в моноклинную. При этой температуре свободная энергия моноклинной фазы GM равна свободной энергии кубической фазы Gk; температура перехода, полученная при нагревании вещества, равна температуре перехода при охлаждении (рис. 6, а).
Однако, как было показано Убберхольдом [41], свободная энергия является функцией не только давления и температуры, но и параметров α и β, характеризующих энергию внутренних напряжений фазы и ее поверхностную энергию, зависящую от состояния соседней фазы. Эти параметры α и β определяются физическим состоянием фаз в системе и существенно различны для зарождающегося зародыша новой фазы и окружающей его матрицы старой фазы.
