Редкоземельные металлы и их полуторные оксиды
Таким образом, для оксидов тербия, диспрозия и гольмия вблизи температуры превращения мы имеем четыре функции свободной энергии.
Превращение при нагревании
1) Gk=fk(p, Т, αk, β k)—свободная энергия кубической матрицы,
2) GM’ = fM(p, Т, α'М, β' М)— свободная энергия зародыша кубической фазы в кубической матрице.
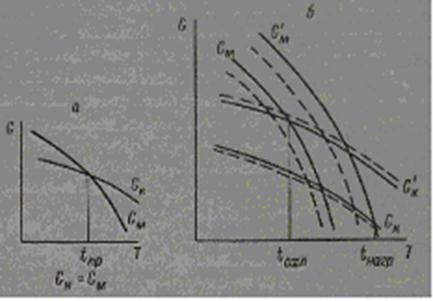
Рис.6. Изменение свободной энергии кубической и моноклинной форм оксидов в зависимости от температуры
а — превращение без гистерезиса; б — превращение с гистерезисом. Пунктиром показано смещение температур фазовых превращений при образовании твердых растворов.
Превращение при охлаждении
3) GМ=fM(p, Т, αM, β M)—свободная энергия моноклинной
матрицы,
4) Gk’ = fk(p, Т, α'k, β' k)—свободная энергия зародыша кубической фазы в моноклинной матрице.
Изменение этих четырех функций Gk, G'M, GM и G’k представлено на рис. 9, б. Условием равновесия будет G'M= Gk при нагревании и G’k = GM при охлаждении. Эта простая схема дает ясное представление о наблюдаемом у этих оксидов явлении гистерезиса: для Tb2О3 Δ(tнагр—tохл)=3000 и для Dy2O3 Δ(tнагр—tохл)=2000 [21]. Кроме этого, для обратимых превращений можно предположить наличие смещении кривых (показано на рис. 6, б пунктиром) свободной энергии в зависимости от совершенства кристаллической решетки каждой из фаз. Однако при высоких температурах и больших скоростях обратимых превращений этот фактор будет оказывать значительно меньшое влияние, чем в случае медленно протекающих необратимых фазовых превращений.
Для однотипных кристаллических веществ термодинамическое условие минимума свободной энергии во многих случаях с достаточной точностью можно заменить условием минимума объема. Критерием объемных изменений, происходящих при образовании соединений, может служить коэффициент компактности структуры q, который равен отношению объема частиц, образующих кристалл, ко всему объему кристалла:
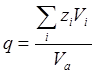
где zi — число частиц сорта i в элементарной ячейке, Vi — объем частицы, Va — объем элементарной ячейки. Из рисунка видно, что коэффициент q изменяется симбатно с изменением — ΔН0 (исключение составляют только оксиды европия и иттербия, склонные к восстановлению при высоких температурах). А-тип структуры является наиболее устойчивым для оксидов элементов с ионным радиусом, большим чем 0.97 А, т. е. для La2О3, Ce2О3, Рr2О3, Nd2О3. Для элементов с меньшим ионным радиусом более устойчивым является В-тип структуры. С-тип структуры является наименее плотно упакованным. Поэтому возможно осуществить С → В-превращение воздействием высокого давления [23]. Однако В-формы оксидов от Но2О3 до Lu2О3 устойчивы только при высоком давлении и переходят обратно в С-формы при снижении давления.
7. СТАБИЛИЗАЦИЯ МЕТАСТАБИЛЬНЫХ ФОРМ ПОЛУТОРНЫХ ОКСИДОВ РЕДКОЗЕМЕЛЬНЫХ ЭЛЕМЕНТОВ
На основании вышеприведенных данных, получить С-форму оксидов легких редкоземельных элементов в состоянии устойчивого равновесия можно только при условии введения в оксид примесей.
Так же как вакансии в кристаллической решетке, примеси оказывают различное влияние на ход полиморфных превращений как в кинетическом смысле (затормаживая или ускоряя переход метастабильных фаз в стабильные), так и в термохимическом (изменяя знак ΔF для реакций перехода одной формы в другую). Вопрос стабилизации того или иного химического соединения сводится к выяснению влияния небольших добавок, не изменяющих типа структуры и характерных свойств данного соединения, но увеличивающих его устойчивость. Нахождение в решетке G-формы оксида гидроксильных групп стабилизирует решетку при низких температурах, малая устойчивость гидратов при высоких температурах практически не допускает повышения температуры перехода С → А-типа.
Другой метод стабилизации различных структурных типов основан на введении в оксид редкоземельного элемента таких добавок, твердые растворы которых с оксидами редкоземельных элементов кристаллизуются в том же типе структуры, но обладают более обширной областью существования. В данном случае термодинамическая устойчивость твердых растворов (или соединений переменного состава, например Рг01;б+ж) определяется величиной изменения энтальпии и энтропии при их образовании.
Можно показать, что в первом приближении энтальпия образования соединения нестехиометрического состава и твердых распоров совпадает с энтальпией образования механической смеси соответствующих стехиометрических соединений, а энтропия их больше, чем у соответствующей механической смеси. Это приведет смещению кривых свободной энергии (рис. 9, б) в зависимости от состава образующегося твердого раствора, а следовательно и к изменению температур фазовых переходов.
Существенным является также влияние метода приготовлена твердых растворов на их структуру. При получении твердых растворов методом соосаждения в аморфном состоянии или разложения легко разлагающихся солей в качестве промежуточного продукта образуются кубические твердые растворы, кристаллизующиеся, в зависимости от состава, в структуре типа флюорита или С-формы оксидов редкоземельных элементов. Относительная устойчивость этих метастабильных форм, а также пути их превращения в устойчивые равновесные фазы сильно зависят от состава твердого раствора. Так, небольшие количества добавок двуокиси циркония к окиси неодима повышают температуру перехода из метастабильной С-формы в А-форму; при больших же количествах двуокиси циркония в твердом растворе метастабильная С-форма сначала переходит в В-форму и только при более высоких температурах образуется равновесный продукт.
Таким образом, вводя в оксиды редкоземельных элементов добавки других оксидов, можно получить твердые растворы, обладающие нужными для практики свойствами и кристаллизующиеся в определенном типе структуры.
8. ЗАКЛЮЧЕНИЕ.
В настоящей работе рассмотрены структура и устойчивость различных форм полуторных оксидов редкоземельных элементов, в частности, европия, а также влияние метода приготовления оксида на его структуру и свойства. На основании изложенного материала можно предложить следующую схему фазовых превращений в окислах редкоземельных элементов (рис. 7).
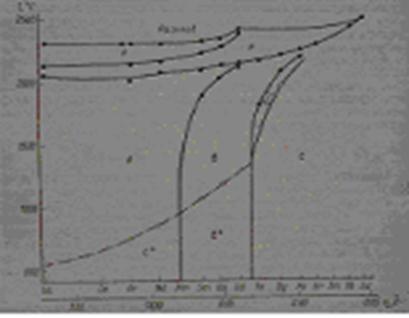
Рис. 7. Диаграмма фазовых превращений в оксидах РЗЭ.
Наблюдаемые на рис. 7 области стабильности различных структурных форм хорошо согласуются с положением, что тип полуторного оксида всецело определяется температурой, давлением и размером катиона. Применение высоких давлений способствует переходу метастабильных С-форм оксида европия В-форму. Температура перехода метастабильной С-формы в устойчивую В-форму зависит от энергии решетки оксидов и возрастает от оксида лантана к оксиду гадолиния.
В дальнейшем необходимо продолжить исследования в области изучения условий получения и свойств твердых растворов на основе оксидов редкоземельных элементов. Кроме этого, необходимо уточнить границы областей существования новых полиморфных модификаций (Н- и Х-форм), присущих европию, а также более детально определить их структуру и механизм превращения.
