Стандартизация измерения рН в неводных средах. Методы определения рН стандартных буферных растворов
lg![]() (2.6.1)
(2.6.1)
Из этого предположения следует, что величина рА определяется выражением
![]() (2.6.2)
(2.6.2)
Такой прием вносит определенную ошибку, обусловленную различием в величинах ![]() протонов и анионов кислот, однако сравнение
протонов и анионов кислот, однако сравнение ![]() для разных кислот показало, что эти величины близки между собой; например,
для разных кислот показало, что эти величины близки между собой; например,
и этиловом спирте ![]() ,
, ![]() ,
, ![]() и т.д. Это же наблюдается и для других растворителей.
и т.д. Это же наблюдается и для других растворителей.
Эксперименты показывают, что величины ![]() ионов кислот в спиртам лишь несколько отличаются от величины:
ионов кислот в спиртам лишь несколько отличаются от величины: ![]() ионов солей. Поэтому нельзя предполагать, что изменения энергии сольватации ионов лиония резко отличается от изменения энергии сольватации остальных катионов. Во всяком случае, величина
ионов солей. Поэтому нельзя предполагать, что изменения энергии сольватации ионов лиония резко отличается от изменения энергии сольватации остальных катионов. Во всяком случае, величина ![]() ионов кислот является вполне однозначной и, вероятно, оценивает изменение кислотности с большей надежностью, чем величины Н0, Н(-), рННас и т.д.
ионов кислот является вполне однозначной и, вероятно, оценивает изменение кислотности с большей надежностью, чем величины Н0, Н(-), рННас и т.д.
2.7 Нахождение единой кислотности рА с помощью ![]() протонов
протонов
Все перечисленные выше методы не позволяют однозначно оценить кислотность неводных растворов в единой шкале. Вопрос об этой шкале может быть решен только на основании данных о величинах химической энергии сольватации протонов в различных растворителях. Эти данные получены на основании подсчетов сумм и разностей химических энергий сольватации ионов в неводных растворах из данных об электродвижущих силах цепей без переноса и с переносом в неводных растворах. Путем экстраполяции величин суммарной энергии сольватации ионов водорода и ионов галогенов (ионы галогеноводородных кислот) и разностей энергий сольватации ионов водорода и ионов щелочных металлов была определена энергия сольватации протона и других ионов в различных растворителях.
При переходе от водного к неводному раствору следует считаться с том, что протяженность шкалы различна для разных растворителей. Для того чтобы оценить абсолютную кислотность, кроме протяженности шкалы нужно знать, как смещено начало шкалы кислотности одного растворителя но отношению к шкале кислотности воды.
Использование ![]() протонов в различных растворителях в качестве единой меры изменения кислотности в разных растворителях однозначно характеризует величину смещения шкал кислотности.
протонов в различных растворителях в качестве единой меры изменения кислотности в разных растворителях однозначно характеризует величину смещения шкал кислотности.
Обозначим начало шкалы для воды через 0; шкала для этилового спирта имеет протяженность 19,3; если ![]() = 4,2, то очевидно, что шкала в этиловом спирте начинается в области —4,2 и заканчивается при рА = 15,1. У метилового спирта
= 4,2, то очевидно, что шкала в этиловом спирте начинается в области —4,2 и заканчивается при рА = 15,1. У метилового спирта ![]() = 3,3, а вся шкала 16,9; шкала для него расположится от - 3,3 до +13,6;
= 3,3, а вся шкала 16,9; шкала для него расположится от - 3,3 до +13,6; ![]() в муравьиной кислоте
в муравьиной кислоте ![]() = 8,6, вся шкала равна 6,1, она расположена между -8,6 и -2,5. У аммиака протяженность шкалы 32,7; она смещена по отношению к воде на 16,4 единицы, начало шкалы будет при рА = 16,4, а конец при рА = 49,1. Из этих сопоставлений следует, что самый щелочной раствор в муравьиной кислоте будет кислее самого кислого раствора в воде и самый кислый раствор в аммиаке щелочнее самого щелочного раствора в воде,
= 8,6, вся шкала равна 6,1, она расположена между -8,6 и -2,5. У аммиака протяженность шкалы 32,7; она смещена по отношению к воде на 16,4 единицы, начало шкалы будет при рА = 16,4, а конец при рА = 49,1. Из этих сопоставлений следует, что самый щелочной раствор в муравьиной кислоте будет кислее самого кислого раствора в воде и самый кислый раствор в аммиаке щелочнее самого щелочного раствора в воде,
Относительное расположение шкалы рНр позволяет оценить отношение между единой кислотностью растворов и величиной рНр. Из рис. 2 следует, что раствор кислоты в спирте, в котором активность а*= (рНр= 0), кислее соответствующего йодного раствори на 4,2 единицы.
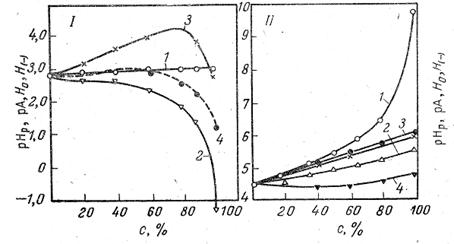
Рис. 2. Изменение рНр (1), рА (2), Н0 (3), и Н(-) (4) растворов HCl (I), и ацетатного буфера (II) в растворах этилового спирта в воде.
Однако не нужно думать, что всякий раствор кислоты в этиловом спирте будет кислее, чем в воде. В действительности рА нормального раствора соляной кислоты в этиловом спирте не будет равна -4,2, так как в нем величина ![]() значительно меньше величины
значительно меньше величины ![]() в воде.
в воде.
Таким образом, в этиловом спирте, с одной стороны, ![]() положителен, и это приводит к уменьшению рА и увеличению кислотности. С другой стороны, lg
положителен, и это приводит к уменьшению рА и увеличению кислотности. С другой стороны, lg ![]() отрицательны и по абсолютной величине больше, чем у воды, а это приводит к увеличению рНр и к уменьшению кислотности. В 1 н. растворе HCl в этиловом спирте величина
отрицательны и по абсолютной величине больше, чем у воды, а это приводит к увеличению рНр и к уменьшению кислотности. В 1 н. растворе HCl в этиловом спирте величина ![]() = 0,157. В результате этого рА 1 н раствора HCl в этиловом спирте будет не -4,2, а значительно меньше (только -3,3), но все же раствор в этиловом спирте значительно кислее, том в воде.
= 0,157. В результате этого рА 1 н раствора HCl в этиловом спирте будет не -4,2, а значительно меньше (только -3,3), но все же раствор в этиловом спирте значительно кислее, том в воде.
Можно сказать, что в этиловом спирте каждый ион лиония становится активнее, по число ионов лиония становится меньше.
Еще резче это будет проявляться в спиртовых растворах уксусной кислоты: с одной стороны, кислотность ионов лиония С2Н5ОН2+ по сравнению с водой увеличивается на 4,2 единицы, но, с другой стороны, константа диссоциации кислоты при переходе от воды к этиловому спирту уменьшается на 5,6 порядка, и оба эффекта в значительной степени компенсируются. Величина рА ацетатного буферного раствора только 5,5. Повышение абсолютной кислотности будет особенно большим только в разбавленных растворах сильных кислот, в которых ![]() = 1.
= 1.
Для иллюстрации на рис. 2 приведены данные для рН и рА разбавленных растворов сильной соляной кислоты (0,002 н. НС1 + 0,008 н. NаCl) и буферных растворов, состоящих из 0,02 н. НАс и 0,01 п. NaAc + 0,0005 н. NaCl в смесях этилового спирта с водой.
Из рис.2 следует, что рНр разбавленных растворов соляной кислоты практически не изменяются при переходе от воды к спиртам. Наоборот, рА резко падают. В отличие от этого рНр ацетатного буфера сильно возрастают в связи со значительным ослаблением силы кислоты Величина рА этого буфера изменяется мало и не уменьшается, как в случае растворов HCl, а несколько возрастает. Из рис, 2 следует также, что ни H0, ни Н(-) не передают действительного хода зависимости единой кислотности с изменением растворителя. Более того, Н(-) одного и того же раствора, измеренная с помощью различных индикаторов [2,4-динитрофенол (Н(-)) и димедон (Н’(-))], расходятся. В этиловом спирте они отличаются более чем на единицу рА. Еще большее расхождение между рА, Н0 и Н(-) для раствором сильных кислот, где они разнятся на 2—4 единицы.
