Проблемы экстракорпорального оплодотворения
Первая беременность, завершившаяся в 1978 г. рождением Луизы Браун, наступила в результате оплодотворения in vitro единственного ооцита, аспирированного в спонтанном цикле, и переноса одного эмбриона в полость матки. В последующих исследованиях была показана низкая эффективность метода при переносе лишь одного эмбриона, которая составляет при работе в естественном цикле не более 8 - 15% из расчета на один перенос эмбрионов. Это привело к необходимости использования лекарственных препаратов, оказывающих стимулирующее действие на фолликулогенез в яичниках в целях получения нескольких преовуляторных ооцитов.
Для стимуляции фолликулогенеза и получения нескольких преовуляторных ооцитов используются гормональные препараты.
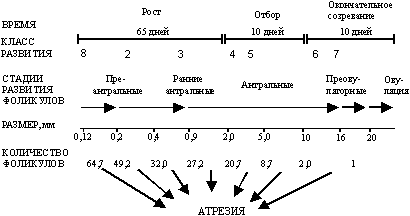
Рис. 5. Цикл развития доминантного фолликула
Стимуляция суперовуляции в современных условиях основана на:
§ стимуляции выделения собственных эндогенных гонадотропинов кломифеном;
§ стимуляции экзогенными гонадотропинами (препараты из мочи менопаузальных женщин - препараты человеческого менопаузального гонадотропина (чМГ), содержащие ЛГ и ФСГ (пергонал, неопергонал, хумегон) или ФСГ (метродин);
§ стимуляции экзогенными гонадотропинами на фоне блокады собственных гонадотропинов препаратами агонистов РГ ЛГ (декапептиды - трипторелин, бусерелин, госерелин, нафарелин и др.). Все эти препараты - синтетические аналоги гонадотропных рилизинг гормонов, и число их постоянно растет. Все они в 50 - 100 раз активнее эндогенных рилизингов. Действие их основано на блокаде собственных гонадотропинов, что позволило некоторым авторам называть этот метод «стимуляция суперовуляции на фоне гипофизэктомии», хотя на самом деле подавляется секреция только гонадотропинов, а не всех тропных гипофизарных гормонов. На фоне снижения уровня собственных гонадотропинов введение экзогенных гонадотропинов позволяет регулировать рост доминантных фолликулов и созревание яйцеклеток.
В повседневной практике используются так называемые «длинная схема» и «короткая схема» введения препаратов.
При длинной схеме введение агонистов начинают в конце фолликулярной фазы предыдущего цикла, под контролем снижения ЛГ в крови. После наступления устойчивого низкого «плато» ЛГ приступают к введению гонадотропных препаратов. При короткой схеме агонисты вводятся с 1-го дня менструального цикла, гонадотропины - с 3-го или 5-го дня цикла.
При любом методе стимуляции суперовуляции постоянно контролируются число фолликулов, темпы их роста и величина фолликулов. До начала стимуляции суперовуляции следует проводить предварительное гормональное обследование, а в период стимуляции - ультразвуковой (УЗ) и гормональный мониторинг. Как правило, исследуется уровень эстрадиола крови и толщина эндометрия. Критериями созревания яйцеклетки, точнее говоря, определением времени, оптимального для забора ооцитов, являются: концентрация эстрадиола не менее 350 пг/мл на 1 фолликул диаметром более 15 мм, толщина эндометрия 0,8 - 1,0 см.
Механизм овуляции, в естественном спонтанном менструальном цикле обеспечивающийся выбросом эндогенного ЛГ, в циклах стимуляции суперовуляции имитируется введением ЛГ-подобного препарата - хорионического гонадотропина (ХГ), получаемого из мочи беременных женщин.
Через 35 - 36 ч после введения овуляторной дозы ХГ (10000 ед.) производится трансвагинальная пункция яичников (ТВП) в целях аспирации зрелых ооцитов. После их оплодотворения in vitro и инкубации в специальной питательной среде через 48 - 72 ч, в зависимости от интенсивности дробления, производится перенос эмбрионов на ранней стадии дробления в полость матки пациентки.
После пересадки эмбрионов рекомендуется вводить поддерживающие дозы хорионического гонадотропина по 1500 ед. и дексаметазона по 0,25 мг, последний подавляет иммунную реакцию отторжения плодного яйца. Препараты вводят до констатации беременности или до срока очередных менструаций (в случае неудачи).
ОСНОВНЫЕ ПРОБЛЕМЫ, ВОЗНИКАЮЩИЕ
ПРИ ПРИМЕНЕНИИ ЭКО И ПЭ
Программа ЭКО и ПЭ сложна в связи с тем, что она многоэтапная, но не все этапы можно объективно проконтролировать. Остановимся на некоторых проблемах, возникающих при применении этого метода.
У женщины вовремя одного естественного менструального цикла можно получить в среднем не более одной яйцеклетки. Манипулируя с яйцеклеткой, ее легко потерять или травмировать, поскольку ее размеры, включая corona radiata, не превышают 500 мк. Яйцеклетка может быть потеряна, например, в пипетке, в капле питательной среды и т. п. Следовательно, необходим резерв клеток.
В связи с этим возникла идея стимуляции так называемой суперовуляции, т. е. получения большего числа яйцеклеток (5 - 10 шт.) за счет применения антагонистов эстрогенов и менопаузальных гонадотропинов ФСГ и ЛГ. Однако увеличение количества яйцеклеток влечет за собой другой отрицательный фактор - некоторые из них могут оказаться неполноценными, с нарушением оогенеза или с хромосомной патологией, а другие могут стать на путь обратного развития в процессе фолликулогенеза. Так что не все полученные яйцеклетки могут быть оплодотворены и нормально развиваться.
Высокая частота самопроизвольных абортов (26,2%) после ЭКО является относительным показателем возможной патологии плодов. Эти данные подтверждаются результатами исследования хромосом яйцеклеток и эмбрионов ранних стадий развития. Известно, что от 35 до 50% нефертилизованных ооцитов в программе ЭКО имеют хромосомные аномалии. Выявлена высокая степень зависимости хромосомных аномалий от возраста беременных женщин. Так, анэуплоидия диагностируется у 47% женщин после 35, лет и у 25% молодых женщин; после кломифена - у 55%, после ЧМГ - у 23%, после чистого ФСГ - у 22%. Значительно чаще хромосомная патология обнаруживается у фрагментированных эмбрионов (33%), чем у нормальных (20%).
Анализ ооцитов и эмбрионов, полученных в программе ЭКО, свидетельствует о том, что основным фактором, обусловливающим высокую частоту хромосомных аномалий, является возраст беременных. Увеличение частоты хромосомной патологии с увеличением возраста имеет тенденцию, аналогичную таковой в популяции, однако показатели этой патологии в 2 раза выше, чем популяционные данные спонтанной фертильности. Высокая частота хромосомных аномалий в нефертилизованных ооцитах свидетельствует о том, что множественная наведенная стимуляцией овуляция, или суперовуляция, сопровождается высокой частотой хромосомной патологии ооцитов, которые созревают в аномальных условиях в отсутствие физиологической селекции и борьбы за существование доминирующего фолликула, который подавляет рост других фолликулов в одном пуле, возможно, не имеющих тенденции к нормальному развитию.
Начато внедрение в практику методики флуорисцентной (in situ) гибридизации (FISH), обеспечивающей преимплантационную диагностику врожденной хромосомной патологии. Отдельные бластомеры извлекаются из эмбриона и проводится их FISH-анализ. Эмбрионы, по которым получено положительное заключение, могут быть перенесены в полость матки для дальнейшего развития, а эмбрионы с обнаруженной патологией не переносятся (в целях профилактики таких заболеваний как гемофилия, синдром Патау, Дауна, Эдвардса, Клайнфельтера, моносомия Шершевского-Тернера).
