Методы измерений
Соотношение (8) называется объединенным газовым законом и формулируется следующим образом: при постоянной массе газа произведение объема на давление, деленное на абсолютную температуру газа, есть величина, одинаковая для всех состояний этой массы газа.
Уравнение состояния для произвольной массы идеального газа (уравнение Клайперона-Менделеева) имеет вид
pV= m • RT, (9)
μ
где т — масса газа; μ — масса одного киломоля газа; R — универсальная газовая постоянная.
Для упрощения процесса измерения давления один из параметров состояния (Т или V) сохраняется постоянным. Тогда давление однозначно определяется по результатам измерения V или Т. Например, при измерении изменений атмосферного давления в баронивелировании нашли применение газовые барометры, принцип действия которых основан на использовании уравнения состояния газа (8) при постоянной температуре, т. е. при постоянной массе газа и неизменной температуре давление обратно пропорционально занимаемому газом объему.
Принципиальная схема газового барометра конструкции Штриплинга изображена на рис. 8. Прибор состоит из двух камер, одна из которых 2 может быть сообщена с атмосферным давлением, а другая 3 замкнута. Обе камеры связаны между собой капилляром, в середине которого находится капля масла 1, выполняющая роль указателя нуля. При равенстве давлений в камерах капля устанавливается на нулевой отметке.
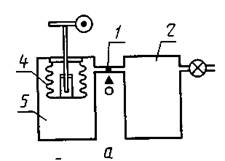
Рис. 8. Принципиальная схема газового барометра
Равенство давлений достигается изменением объема камеры 3 посредством перемещения сильфона 4 с помощью винта и червячной передачи с отсчетом числа оборотов червяка по цифровому счетчику. При погрешности термостатирования 0,001°С изменения давления фиксируются с погрешностью менее 0,5 Па.
В дифференциальном газовом барометре системы Д.И. Менделеева (рис. 9) изменение атмосферного давления определяется комбинированным методом. Барометр состоит из замкнутого сосуда 1, соединенного с давлением окружающего воздуха при помощи V-образного жидкостного манометра 2.
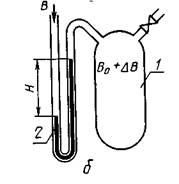
Рис. 9. Дифференциальный газовый барометр
Барометр основан на уравновешивании изменений атмосферного давления как столбом жидкости, так и сжатием (расширением) газа в замкнутом сосуде по закону Бойля-Мариотта. Как и ранее, необходимо тщательное термостатирование сосуда 1 или введение температурной поправки, равной 0,37 % на 1°С.
Следует отметить, что рассмотренные выше газовые барометры в связи с появлением высокоточных деформационных барометров аналогичного назначения в настоящее время практически не применяются. В отличие от этого в области вакуумных измерений указанный принцип находит широкое применение. Компрессионные („компрессия" — сжатие) и экспансионные („экспансия" - расширение) манометры являются основными средствами воспроизведения к передачи единицы давления в области вакуумных измерений в диапазоне от 10-3 до 103 Па (10-5 -10 мм рт. ст.).
2.2. Косвенные методы, основанные на фазовых переходах
Известно, что любое вещество в зависимости от давления и температуры может находиться в различных агрегатных состояниях (твердой, жидкой и газообразной фазах). Типовая диаграмма состояний в координатах р и Т представлена на рис. 10. Кривыми линиями изображены границы между различными фазами (кривые равновесия фаз), соответствующие давлениям и температурам, при которых из одной фазы в другую переходит одинаковое число молекул.
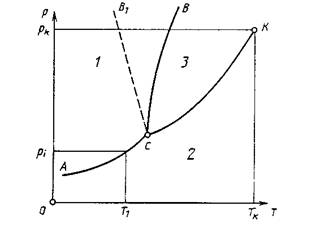
Рис. 10. Типовая диаграмма состояний
При этом кривая СК выражает зависимость от температуры давления насыщенного пара над жидкостью; кривая АС - давления насыщенного пара над твердым телом, кривая ВС - температуры плавления от давления. Например, при давлении р1 и температуре Т1, будет наблюдаться равновесие твердой 1 и газообразной 2 фаз. Если при той же температуре Т1, давление понизить, то начнется переход твердой фазы в газообразную. Этот процесс называется возгонкой или сублимацией („сублимаре" — возносить). Аналогично на границе ВС происходит плавление твердой фазы (кристаллизация жидкой фазы 3), а на границе СК - кипение жидкой фазы (конденсация газообразной фазы). Необходимо отметить также две особые точки. Тройная точка С, находящаяся на пересечении всех трех кривых равновесия фаз, характеризует состояние вещества, когда находятся в равновесии одновременно твердая, жидкая и газообразная фазы. Критическая точка К соответствует критической температуре Тк и критическому давлению рк, при которых теряется всякое различие между жидкостью и ее паром, а граница между ними исчезает.
Указанные выше кривые равновесия фаз и тройная точка используются в косвенных методах определения давления по результатам измерения температуры в равновесных точках (в области температурных измерений, наоборот, температура определяется по результатам измерения давления).
Диаграмма состояний дает наглядное представление о выборе того или иного фазового перехода в зависимости от определяемого давления. Кривая плавления ВС немного отклоняется от вертикали к оси абсцисс, т. е. температура плавления имеет небольшую чувствительность к давлению. Так, температура плавления льда изменяется на 1 К при изменении давления на 13 МПа (следует отметить, что в отличие от большинства веществ температура плавления льда понижается при повышении давления - штриховая линия СВ на рис 10) , Поэтому кривые плавления используются в косвенных методах определения высоких и сверхвысоких давлений. Процесс сублимации (кривая АС) происходит, как правило, при низких температурах и давлениях, что позволяет его использовать при определении давления в области вакуумных измерений. И, наконец, фазовый переход жидкость—пар (кривая СК) наиболее удобен для области средних давлений помимо указанного, пои выборе того или иного фазового перехода необходимо учитывать физические свойства применяемого вещества.
В области измерения высоких и сверхвысоких давлений его значение воспроизводится по кривой плавления ртути, полуэмпирическое уравнение которой получают по результатам исследований сравнением с эталонным поршневым манометром. Это позволяет построить непрерывную шкалу давлений, по которой градуируются средства измерений высоких и сверхвысоких давлений низшей точности.
В области средних давлений, где успешно применяются высокоточные средства измерений, основанные на прямых методах, использование косвенных методов нецелесообразно. Однако представляет интерес, получивший распространение в первой половине нашего века простой способ измерения атмосферного давления, основанный на фазовых переходах „жидкость—пар" (кривая СК на рис. 10), который легко может быть продемонстрирован в любой, даже школьной, лаборатории.
2.3. Косвенные методы, основанные на изменении физических свойств измеряемой среды
