Смола
Образование новолаков в присутствии щелочных катализаторов
Поликонденсацией в присутствии оснований в зависимости от мольного соотношения реагентов и условий реакции могут быть получены или резолы, или новолаки. Новолаки получаются при высоких температурах и избытке фенола. Макромооекулы этих
новолаков из-за содержания в них трисоксиметилфенола разветвлены сильнее, чем новолаки, полученные в кислой среде. Следовательно, в процессе образования новолака в присутствии оснований соотношение фенола и формальдегида уменьшается.
-10-
Смолу, полученную взаимодействием двух молей фенола с 1 молем формальдегида в присутствии NH3 или MgO, подвергают последующей термообработке при 160°С. При этом из фенолоспиртов и избыточного фенола образуются продукты поликонденсации, содержащие метиленовые связи.
Образование резолов
В состав резолов входят в основном оксиметилфенолы, диоксидифенилметаны и диоксидибензиловые эфиры. На первой стадии получения резола в присутствии щелочного катализатора происходит нуклеофильпое присоединение иона фенолята (I) к формальдегиду (II), причем начало образования резола аналогично образованию альдоля.
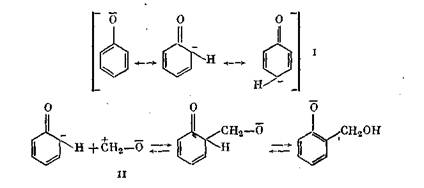
Щелочная конденсация резола про гекает через стадию образования иона карбония — по аналоги! с конденсацией в присутствии кислого катализатора. Образование иона карбония может сопровождаться возникновением переход ного комплекса, содержащего водородные связи.
На скорость реакции влияет энергия отрыва протона от орто-или пара-положения фенола, которая, по-видимому, у метилолфено-лов меньше, чем у фенола. Поэтому конденсация метилолфенолов друг с другом протекает быстрее, чем их конденсация с фенолом.
В щелочной среде фенол может присоединять до трех молекул формальдегида. При мольном соотношении фенол : формальдельгид 1 : >• 1 в щелочной среде образуются метилолфенолы, соединенные метиленовьши и диметиленэфирными группами. Содержание метилольных, метиленовых и диметиленэфирных групп зависит от мольного соотношения реагентов, природы катализатора, концентрации исходных компонентов, температуры и продолжительности реакции.
Низкомолекулярныс резолы
В умеренных условиях (температура около 70 °С), при избытке формальдегида (1,5—2 моля на 1 моль фенола) и соответствующих количествах гидроокисей щелочных и щелочноземельных металлов образуются относительно низкомолекулярные, водорастворимые смолы, содержащие преимущественно метилольные группы. В их состав входят различные одно- и двухядерные фенолоспирты с высоким содержанием метилольных групп (обладающие поэтому высокой реакционной способностью), свободные фенол и формальдегид.
Растворимость низкомолекулярных резолов в воде по мере повышения температуры уменьшается (метилольные группы превращаются в диметиленэфирные и метиленовые), на что указывает повышение вязкости. Вязкость повышается также при длительном хранении. Низкомолекулярные резолы применяются в качестве пропиточных смол, клеев, связующих для древесины, тканей, бумаги, стекло- и шлаковаты.
-11-
Высокомолекулярные резолы
Для высокомолекулярных резолов характерно высокое содержание метиленовых групп, а их структура аналогична структуре новолаков. Различие между ними в том, что у резолов относительно высокое содержание метилольных и диметиленэфирных групп.
Образование высокомолекулярных смол происходит уже при небольшом избытке формальдегида (1—1,5 моля на 1 моль фенола), незначительных количествах гидроокисей щелочных металлов и повышенных температурах (выше 70 °С). Эти смолы легко и быстро при незначительном выделении летучих продуктов конденсации (Н20, СН20) переходят в состояние резита.
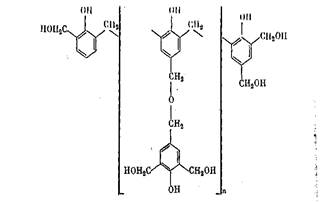
Высокомолекулярные резолы нерастворимы в воде, но растворяются в спиртах и кетонах. Они применяются в качестве литьевых смол, защитных пленок, связующих для слоистых материалов, пресс-масс. Ниже в качестве примера приведена формула высокомолекулярного резола:
ОТВЕРЖДЕНИЕ И ОТВЕРДИТЕЛИ
Взаимодействие фенола с альдегидами протекает, как правило, медленно. Поэтому для ускорения реакции и проведения ее в определенном направлении используют катализаторы. Общей особенностью поликонденсации как с кислыми, так и с основными катализаторами является присоединение формальдегида к фенолу с образованием метилольных групп. Кислые катализаторы не только способствуют образованию метилольных групп, но и ока-
азывают влияние на дальнейшее, также зависящее от температуры протекание реакции между первичными фенолоспиртами и фенолами или между фенолоспиртами.
Кислыми катализаторами могут служит НС1, Н2S04, Н3Р04, НСООН, СН3СООН, молочная, щавелевая, сульфаниловая, три-хлоруксусная, n-толуолсудьфокислота, КН4С1, ZnС12, МgС12 и другие хлориды металлов кислого характера. Щелочными катализаторами служат
гидроокиси щелочных или щелочноземельных металлов, NН3, некоторые амины.
Как уже отмечалось, поликонденсацию в любой момент можно приостановить и при необходимости продолжить. Отверждение — это как бы доведение процесса поликонденсации до стадии, на которой достигаются необходимые свойства продукта. Стадии поликонденсации классифицируют по общим свойствам смол:
стадия А — резолы или новолаки, плавкие и растворимые;
стадия В — резитолы, еще формующиеся при нагревании и способные к набуханию;
стадия С — резиты — конечные продукты поликонденсации, неплавкие, нерастворимые.
-12-
Время, необходимое для перехода смолы из жидкого в вязкое, каучукоподобное состояние В,
обозначают временем В, а для перехода в неплавкое состояние С — временем С.
Скорость отверждения определяется, в первую очередь, реакционной способностью фенолов по отношению к формальдегиду и увеличивается в ряду: фенол — м-крезол — 3,5-ксиленол. Время В и С дает возможность сравнивать свойства различных смол при отверждении, но не служит абсолютной мерой продолжительности отверждения.
При отверждении резолов при нагревании (150—180 °С) образуются в основном метиленовые и диметиленэфирные мостики. Последние чувствительны к высоким температурам — при 200 °С и выше протекают реакции превращения, сопровождающиеся изменением цвета продукта до темно-коричневого. Эти реакции уже не влияют на рост цепи. При этом наблюдается преимущественно окислительное восстановление хинонметидов, появляются типичные для подобных процессов группы и соединения: этиленовые (—СН2—СН2—), виниленовые (—СН=СН—), циклические хинолэфиры, а также метальные и формильные концевые группы. При температурах выше 300 °С начинается деструкция.
В случае отверждения резолов кислотами при рН среды выше определенного значения отверждения практически не происходит. Такое значение рН называется предельным, или пороговым, и является характеристической конбтантой всех резолов, отверждающихся при нагревании.
