Смола
Ниже приведена возможная структура отвержденной смолы (кислое отверждение):
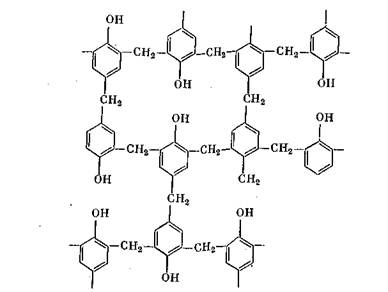
В ряде случаев наблюдается недостаточное отверждение смол, что отрицательно сказывается на их механической прочности и теплостойкости. В полимерной сетке
появляется много слабых мест, которые могут значительно ухудшать свойства изделий. Этот фактор, по-видимому, объясняет часто наблюдаемые большие расхождения между теоретическими и практическими значениями прочности. Возникновение слабых мест может быть обусловлено, во-первых, пространственными затруднениями во-вторых, наличием конденсационной воды, которая может приводить к появлению «дырок» ( дефектов структуры). Кроме того, чем больше молекула, тем меньше вероятность вступления в реакцию всех функциональных групп.
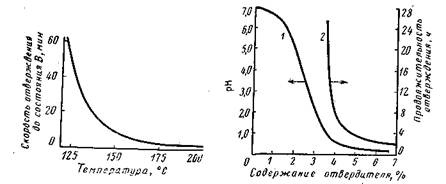
Влияние температуры на скорость отверждения резола показано на рис. 2.1, а на рис. 2.2 — влияние концентрации кислого-отвердителя на продолжительность отверждения и рН резола.
2.1.Зависимость скорости отверждения 2.2. Зависимость продолжительности отверждения и рН резола
от температуры отверждения и рН резола от содержания отвердителя.
-13-
Для новолаков в качестве отвердителей используют гекса-метилентетрамин (уротропин), параформальдегид, а также мети-лолсодержащие феноло-, карбамиде-, меламино- и дицианди-амидоформальдегидные продукты поликонденсации или смесь уротропин — борная кислота (15 : 5) [42]. Среди них наибольшее промышленное применение получил уротропин. Его образование при взаимодействии NН3 с СН20 проходит с выделением воды:
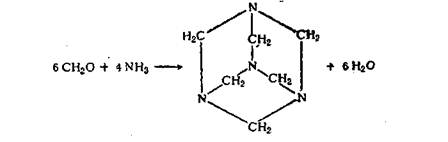
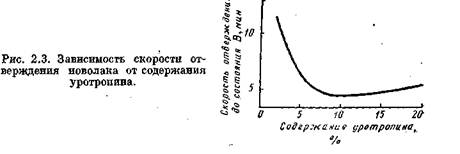
При отверждении уротропином выделяется лишь небольшое количество NH3, но не вода, что исключает возникновение слабых мест в полимерной сетке. Часть аммиака, как указано выше, превращается в диметиленамишше, а также в триметиленаминные группы. При большом избытке реакционноспособных атомов водорода в фенольных ядрах почти весь азот уротропина выделяется в форме NН3- Влияние уротропина на скорость отверждения новолака показано на рис. 2.3.
Глава 4
Физико-химические основы получения олигомеров ФФАП
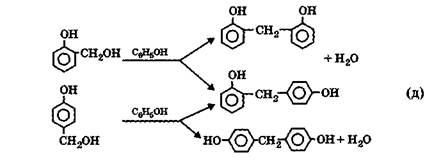
Олигомеры получаются поликонденсацией фенола и формальдегида в водной среде в присутствии катализаторов кислотного или щелочного характера. Реакция протекает через стадию оксиметилирования в орто- и параположения фенольногоядра с образованием соответствующих орто- и параметилолфенолов (оксибензиловых спиртов)
|
|
(а)
Дальнейшее течение реакции, следовательно, строение и свойства получаемых олигомеров, зависят от мольного соотношения фенола и формальдегида и природы
-14-
катализатора, то есть от рН среды.
В щелочной среде и при избытке формальдегида протекает и далее преимущественно реакция оксиметилирования и образуется смесь фенолоспиртов в соответствии со схемой:
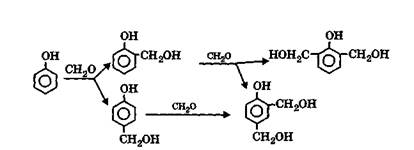 (в)
(в)
При этом, на практике условия реакции выбираются так, чтобы избежать образования триметилолфенола и получить олигомеры линейного строения.
Образовавшиеся по схеме (б) фенолоспирты вступают в акцию поликонденсации между собой или с фенолом, образуя димеры, которые затем взаимодействуют с фенолоспиртам образованием олигомеров более высокой степени поликонденсации. Пример поликонденсации на данной стадии показан схеме (в).
Общее уравнение поликонденсации фенола и формальдеги да в щелочной среде может быть представлено так:
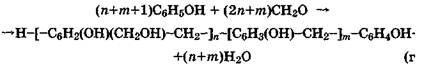
где: п — среднее число звеньев, содержащих метилольную группу,
т — среднее число звеньев, не содержащих метилольную группу.
Таким образом, образующиеся в щелочной среде олигомеры представляют смесь линейных и разветвленных полимергомо логов, содержащих в макромолекуле реакционноспособные метилольные группы. Среднее число фенольных ядер в макро молекуле олигомера (п + т + 1) составляет 4—10, а число метилольных групп 2—5. Подобные олигомеры при нагревании способны к реакциям сшивания за счет содержащихся в них метильных групп, то есть представляют термореактивные олиго-ры. Они получили название резолов.
В кислой среде и при избытке фенола образовавшиеся по схе-ме(а) фенолоспирты
реагируют с фенолом с образованием диоксидифенилметанов по схеме:
|
|
Так как в этих условиях скорость поликонденсации значительно выше скорости оксиметилирования, то диоксидифенилметаны реагируют преимущественно с фенолоспиртами, например по схеме:
-15-
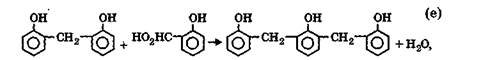
в результате чего образуются олигомеры преимущественно линейного строения с незначительным содержанием метилольных групп.
Общее уравнение поликонденсации фенола и формальдегида в кислой среде может быть представлено таким образом:
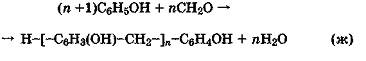
где: n = 4—8.
Подобные олигомеры практически не содержат метилольных групп и не способны к реакциям сшивания при нагревании без добавления специальных отвердителей, то есть являются термопластичными олигомерами. Они получили название новолаков.
Реакции оксиметилирования (а и б) и реакции конденсации (в, д и е) практически необратимы. Константа равновесия процесса поликонденсации, условно выражаемого уравнением:
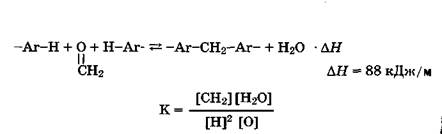
имеет порядок 103—104, то есть поликондепсация неравновес ная. Поэтому процесс получения олигомерон осуществляется в водном растворе формальдегида. Скорость поликонденсации зависит от температуры и концентрации катализатора (рН сре ды), а молекулярная масса получаемого олигомера от времени.
Производство новолачных олигомеров
Феноло-формальдегидные новолачные олигомеры в промышленности производятся
периодическим и непрерывным способами. Технологический процесс включает следующие стадии: дозировка сырья, поликонденсация, сушка олигомера охлаждение и измельчение готового продукта.
Мольное соотношение фенола и формальдегида составляет от 1:0,78 до 1:0,86. В качестве катализатора используется соляная кислота в количестве 0,2—1,5 мае. долей на 100 мае. долей фенола, что обеспечивает рН среды в пределах 1,5—1,8. На рис. 18.4 представлена технологическая схема производств новолачных олигомеров непрерывным способом с использованием реактора поликонденсации колонного типа.