Технология нуклеофильного замещения функциональных групп в органических соединениях
Выход фенола на стадии плавления — 96% от теоретического. При улавливании фенола из паров, выделяющихся в плавильном котле, выход на стадии плавления можно повысить до 97—98%.
Выход на стадии гашения 99% от теоретического. При улавливании фенола из паров, выделяющихся из гасителя, выход может достигать 99,5—99,8%.[14]
Производство резорцина. Щелочное плавление сухих м-дисульфоната бензола и едкого натра проводят в стальном литом котле емкостью около 1 м3. Котел снабжен мощной (64 кВт) лопастной мешалкой, укрепленной в подпятнике и вращающейся со скоростью 20 об/мин. Выгрузка плана производится через широкое выгрузочное отверстие в днище котла. Обогрев котла электрический. Особая трудность аппаратурного оформления процесса получения резорцина связана с тем, что в процессе щелочного несколько раз меняется консистенция реакционной массы. Загружаемая в аппарат порошкообразная смесь при 210—220 ºС превращается в вязкую пластичную массу, которая разжижается при температуре выше 220°С; при температуре 290 °С масса снова густеет и снова превращается в порошкообразный твердый продукт, который при 310 ºС превращается в тестообразную массу, а при 340 ºС затвердевает. Эти изменения вязкости реакционной массы обусловлены протеканием процесса в несколько стадий. Вначале замещается одна сульфогруппа и из реакционной массы отгоняется вода, а затем происходит замещение второй сульфогруппы и отгонка образовавшейся воды:
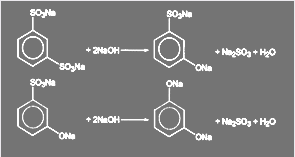
Резорцин, в отличие от фенола, хорошо растворим в воде и в водных растворах солей, а потому не осаждается при подкислении растворенного в воде плава. В связи с этим после отделения сульфита из нейтрализованного раствора плава резорцин извлекают экстракцией органическими растворителями.[15]
3. Особенности техники безопасности при проведении процессов нуклеофильной замены галогена и сульфогруппы
Во многих случаях процессы нуклеофильного замещения галогена (особенно при замене на -ОН, -ОR, -NН2, -NНR-группы) проводят при температурах более высоких, чем температура кипения реагентов или среды. Поэтому в тех случаях, когда реакцию проводят в жидкой фазе, приходится использовать автоклавы или другие аппараты для проведения процессов под давлением.[16]
Установка и эксплуатация автоклавов, а также проектирование и эксплуатация автоклавных отделений должны проводиться в соответствии с требованиями "Правил устройства и безопасной эксплуатации сосудов, работающих под давлением". При этом необходимо установить безопасный режим работы автоклава, в том числе допустимые скорости повышения и снижения температуры и давления.
Аппараты для проведения технологических процессов с применением сильнодействующих и ядовитых веществ (цианиды, метиловый спирт и т. д.) должны размещаться в боксах, укрытиях, камерах, оборудованных местными отсосами и необходимыми устройствами по предупреждению распространения вредностей или в отдельных изолированных помещениях.[17]
К работе с метанолом допускаются лишь лица, прошедшие специальный инструктаж. При работе с метанолом необходимо руководствоваться "Правилами по перевозке, хранению и применению метанола", а также "Правилами безопасности для производства медицинской промышленности". Получение метанола со склада, хранение и расходование его проводятся под строжайшим контролем ответственных лиц, так как метанол является сильным ядом. Запрещается совместное хранение (в одном складе) метанола с этиловым спиртом. Все оборудование, в котором происходят процессы с применением метанола, должно быть герметизировано и снабжено отсосами. Лабораторные работы с применением метанола могут проводиться только в вытяжных шкафах. Для работы в заводских цеховых лабораториях метанол может выписываться в размере суточной потребности, остаток должен сдаваться на склад или храниться в опечатанном шкафу.[18]
Применение метанола допускается лишь в тех случаях, когда он не может быть заменен менее токсичным веществом.
Во многом аналогичные правила установлены для работы с цианистыми соединениями и соединениями мышьяка.
Соответствующие отделения должны иметь поглотительные установки для обезвреживания токсичных выделений, средства для контроля за состоянием воздушной среды, индивидуальные средства защиты и т. д.
В отделениях цианирования не допускается устройство заглубленных аппаратов и приямков. Маточники, сточные воды, воды от промывки аппаратов и смыва полов должны обезвреживаться на локальных установках.
В помещении цианирования должны находиться не менее двух человек — аппаратчик и мастер — для наблюдения за процессом и оказания необходимой помощи в случае аварии.
Во всех случаях применения токсичных соединений или соединений, образующих взрыво-пожароопасные смеси с воздухом должна строго контролироваться герметичность оборудования. Необходимо помнить, что амины являются нервными и кровяными ядами, спирты обладают наркотическим действием, щелочь при попадании на кожу (особенно на слизистую оболочку) вызывает химический ожог, вдыхание пыли Nа2 SО3 и других солей вызывает раздражение дыхательных путей и т. п.[19]
Аммиак, спирты и многие растворители, используемые в процессах замещения галогенов, образуют взрыво- и пожароопасные смеси с воздухом.
Многие фенолы и амины являются сильными нервными и кровяными ядами.
Заключение
нуклеофильный галоген сульфогруппа синтез
Материал, рассмотренный в данной работе должен помочь будущему химику – технологу освоить методы тонкого органического синтеза, правильно выбрать оптимальную химическую схему синтеза целевого продукта. Данная работа посвящена главным образом рассмотрению нуклеофильной замены галогена и сульфогруппы на другие функциональные группы. Реакции нуклеофильного замещения галогена являются весьма важными и распространенными в органическом синтезе и синтезе лекарственных веществ, а так же витаминов. Они используются в синтезе димедрола, фенацетина, азалина, сульфапиридазина, сульфалена, сульфадиметоксина, диакарба, азафена, папаверина, левомицетина, витаминов В2 и В6. Так же этот метод имеет большое значение в синтезе пептидов, антибиотиков, модификаций сахаров. [20]
Список использованных источников
1 Белобородов В.Л., Зурабян С.Э., Лузин А.П., Тюкавкина Н.А. Органическая химия. – М.: Дрофа, 2002. – Кн.1 : Основной курс. – 640 с.: ил.
2 Беляев Е.Ю. Практическая органическая химия. — Изд-во Красноярского университета, 1996. — 439с.
3 Березин Б.Д., Березин д.Б. Курс современной органической химии. —Химия, 1999. — 768 с.
4 Джальберт Э. Сульфирование органических соединений. — М.: Химия,—414 с.
5 Ингольд К Теоретические основы органической химии. — М.: Мир,
1973. — 1055 с.
6 Карапетьянц М.Х., Дракин С. И. Общая и неорганическая химия. —
4-е изд. — М.: Химия, 2000. — 592 с.
7 Липович В.Г., Полубенцева М. Ф. Алкилирование ароматических углеводородов. — М.: Химия, 1985. — 272 с.
8 Лисицын В.Н. Химия и технология промежугочных продуктов. — М.:Химия, 1987. — 368 с.
