Физико-химические основы адсорбционной очистки воды от органических веществ
При сорбции из водных растворов, а в особенности из таких многокомпонентных систем, как сточные воды, этот пик размыт. Например, при доочистке сточных вод максимальные значения сорбционной емкости достигались при 35 – 60ºС. Емкость угля при 0 – 10 и выше 75 – 80ºС была в 1,5 – 2 раза ниже. В других случаях оптимальная температура может быть иной. Есть данные о том, что с повышением температуры значительно улучшается кинетика адсорбции при доочистке высококонцентрированных вод, что связано с перестройкой молекул в растворах, разрушением ассоциатов воды и сорбируемого вещества, снижением вязкости раствора. Изменение сорбируемости различных веществ на АУ при нагревании неодинаково.
Многокомпонентность состава природных и сточных вод приводит к тому, что показатели сорбции малого (до 5%) или очень большого (более 95%) количества загрязнений от общего отличаются от средних. Обычно это выражается в завышенных показателях сорбции небольшой части хорошо сорбируемых примесей и, наоборот, в низких показателях при высокой степени очистки от плохо сорбируемых веществ. Последнее приводит к тому, что при сорбции в статических условиях при необходимости повысить эффект очистки воды до 92 – 95% дозу АУ следует резко увеличить. [5]
4. Изотермы адсорбции. Уравнение Лэнгмюра. Уравнение фрейндлиха
Основные сведения о сорбционных свойствах материала и характере адсорбции на нем определенных веществ могут быть получены из изотерм адсорбции, характеризующих зависимость сорбционной способности ![]() от концентрации
от концентрации ![]() (или давления
(или давления ![]() ) сорбируемого компонента при постоянной температуре:
) сорбируемого компонента при постоянной температуре: ![]() для жидкой фазы или
для жидкой фазы или ![]() для газов. Брунауэр, Эммет и Теллер выделили пять основных типов изотерм сорбции (рис 1). Выпуклые участки изотерм /, II и IV типов (Лэнгмюровская адсорбция) указывают на наличие в сорбентах микропор, но, кроме того, сорбенты II и IV имеют еще и макропоры. Изотермы III и V типов встречаются реже и описывают сильное межмолекулярное взаимодействие в веществе сорбата. Крутизна изотермы I типа характеризует размер микропор сорбентов: а — ультрамикропористых, б — микропористых. Изотерма !Vб принадлежит переходно-пористому сорбенту; 1Vв — однородно макропористому, а 1Vа — со смешанной структурой.
для газов. Брунауэр, Эммет и Теллер выделили пять основных типов изотерм сорбции (рис 1). Выпуклые участки изотерм /, II и IV типов (Лэнгмюровская адсорбция) указывают на наличие в сорбентах микропор, но, кроме того, сорбенты II и IV имеют еще и макропоры. Изотермы III и V типов встречаются реже и описывают сильное межмолекулярное взаимодействие в веществе сорбата. Крутизна изотермы I типа характеризует размер микропор сорбентов: а — ультрамикропористых, б — микропористых. Изотерма !Vб принадлежит переходно-пористому сорбенту; 1Vв — однородно макропористому, а 1Vа — со смешанной структурой.
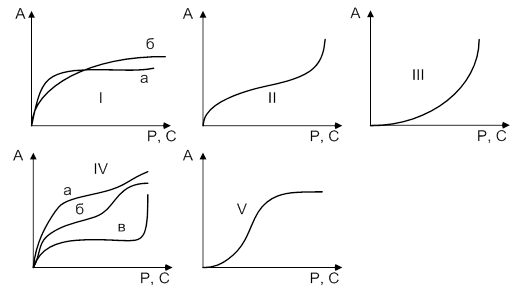
Рис. 1. Типы изотерм сорбции по БЭТ
Чем круче изотерма, тем мельче микропоры. Предельное значение такой адсорбции Апр соответствует покрытию поверхности мономолекулярным слоем. Вогнутые участки указывают на наличие макропор. [4]
Изотерма мономолекулярной адсорбции на микропористых сорбентах обычно имеет вид, показанный на рис. 2. Эта кривая имеет два прямолинейных участка – при малых и больших значениях равновесной концентрации адсорбата. Как адсорбция паров, так и адсорбция из растворов осуществляется в области пор с радиусом 0,5 – 1,6 нм.
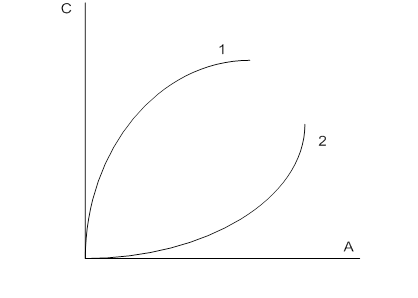
Рис.2. Изотермы адсорбции:
1 – выпуклая (Лэнгмюра);
2 – вогнутая (на макропорах)
Для аналитического описания изотермы мономолекулярной адсорбции чаще всего используется уравнение Лэнгмюра:
![]() (5)
(5)
где ![]() – удельная адсорбция, ммоль/г:
– удельная адсорбция, ммоль/г: ![]() – предельная адсорбция, ммоль/г;
– предельная адсорбция, ммоль/г; ![]() – равновесная концентрация адсорбата, ммоль/л;
– равновесная концентрация адсорбата, ммоль/л; ![]() – адсорбционная константа.
– адсорбционная константа.
Уравнение Лэнгмюра описывает изотерму адсорбции во всех областях равновесных концентраций. При малых концентрациях, когда ![]() , формула упрощается и приобретает вид:
, формула упрощается и приобретает вид:
![]() (6)
(6)
Для условий, когда ![]() , формула (5) дает независимость адсорбции от концентрации:
, формула (5) дает независимость адсорбции от концентрации:
![]() (7)
(7)
Уравнение (5) может быть преобразовано в линейную форму путем его умножения на ![]() и последующего деления на
и последующего деления на ![]() , в результате чего оно приобретает вид:
, в результате чего оно приобретает вид:
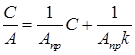 (8)
(8)
Уравнение (8) представляет собой уравнение прямой. По этой зависимости определяют величину предельной адсорбции (рис.3).
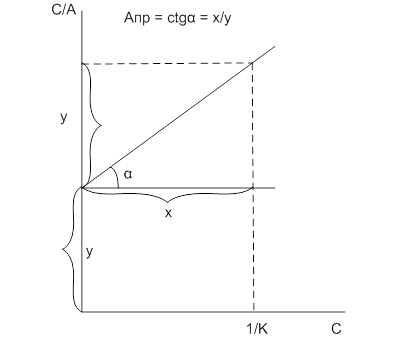
Рис. 3. Схема определения констант в уравнении Лэнгмюра
В области промежуточных равновесных концентраций (на небольших участках изменения концентрации адсорбата) зависимость адсорбции от концентрации часто может быть описана уравнением Фрейндлиха, в основе которого лежит допущение, что изотерма адсорбции является параболой:
![]() (9)
(9)
где ![]() и
и ![]() – константы. Константа
– константы. Константа ![]() зависит от природы адсорбента и адсорбата и колеблется в широких пределах. Константа
зависит от природы адсорбента и адсорбата и колеблется в широких пределах. Константа ![]() возрастает с увеличением длины углеводородного радикала ПАВ, т.к. при этом возрастает адсорбционная способность вещества. Показатель
возрастает с увеличением длины углеводородного радикала ПАВ, т.к. при этом возрастает адсорбционная способность вещества. Показатель ![]() колеблется в пределах 0,1 – 1 и зависит от температуры и природы адсорбата.
колеблется в пределах 0,1 – 1 и зависит от температуры и природы адсорбата.
В логарифмированном виде уравнение Фрейндлиха представляется прямой (рис. 13):
![]() (10)
(10)
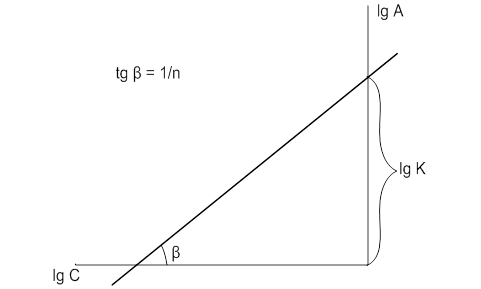
Рис. 4. Схема определения констант в уравнении Фрейндлиха
Отрезок, отсекаемый прямой на оси ординат, равен ![]() , а тангенс угла наклона прямой к оси абсцисс равен
, а тангенс угла наклона прямой к оси абсцисс равен ![]() . [3]
. [3]
5. Расчет изотермы адсорбции молекулярно-растворенных органических веществ на активных углях без экспериментальных измерений
Одна из основных задач при определении технологического режима адсорбционной установки – это расчет условий адсорбционного равновесия, т.е. расчет изотермы адсорбции. Зависимость количества адсорбированного вещества от равновесной концентрации в растворе необходимо знать при расчете кинетики и динамики адсорбции, а также при расчете удельного расхода адсорбента при любом способе технологического оформления адсорбционного процесса.
