Физико-химические основы адсорбционной очистки воды от органических веществ
Комплексный экспресс-анализ адсорбентов для выяснения их практической пригодности для очистки воды во всех случаях включает определение кинетики адсорбции и адсорбционной емкости в стандартизированных условиях. Ускоренный анализ большого числа образцов АУ возможен в два этапа:
– определение кинетики адсорбции (например, по нитрофенолу) по 2 – 5 точкам в статических условиях при С – 0,8 и 4 мг/л и τк = 3 – 24 ч;
– определение выходной кривой при адсорбции в динамических условиях.
Несколько более подробное изучение сорбции может включать три этапа:
1. построение изотермы адсорбции – 4,5-минутное встряхивание предварительно измельченной навески адсорбента со 100 мл воды; 5-минутное фильтрование под вакуумом для отделения сорбента от воды;
2. адсорбция в динамическом полунепрерывном режиме – 1,00 г ГАУ помещают в колбу Эрленмейера с мешалкой, куда подают 20 мл/мин воды; продолжительность опыта 120 мин; отбор проб на анализ через каждые 15 мин;
3. адсорбция в колонках с плотным слоем – τк = 7,5 мин: Нр = 760 мм; Тф = 5 – 30 сут; проскок наступает через 0,1 – 0,2Тф.
Результаты такого исследования отличаются от промышленных, в которых адсорбционную емкость ГАУ определяли экстракцией загрязнений из АУ хлороформом лишь на 5 – 10%. [7]
6.1 Влияние природы поверхности и пористости углеродных адсорбентов на молекулярную адсорбцию органических веществ из водных растворов
Распространенной примесью активных углей является кислород. Его содержание колеблется от 1 до 15% (в окисленных активных углях). По крайней мере 25% всего кислорода, содержащегося в активных окисленных углях, входит в состав поверхностных оксидов, обладающих свойствами объемных соединений с соответствующими функциональными группами.
Более распространены и изучены кислотные кислородсодержащие поверхностные группы. Исследование адсорбции фенола, анилина и n-нитроанилина на образцах ацетиленовой сажи и активного угля КАД с различным содержанием поверхностных функциональных групп показало, что поверхностные кислородсодержащие группы угля и сажи существенно не участвуют во взаимодействии молекул ароматических производных с поверхностью углеродных адсорбентов.
Все адсорбенты по характеру пористости подразделены А.В. Киселевым на четыре типа: непористые, однородно-крупнопористые, однородно-мелкопористые и неоднородно-пористые. Только непористые и однородно-крупнопористые адсорбенты могут быть достаточно полно охарактеризованы удельной поверхностью и только для них могут быть вычислены абсолютные изотермы адсорбции, где величина адсорбции отнесена к единице поверхности.
Наиболее систематическое исследование зависимости характера адсорбции от размеров пор адсорбента выполнено М.М. Дубининым и его сотрудниками. На основании этих работ все поры углеродных адсорбентов можно разделить на три группы по величине их эффективного радиуса (эффективный радиус равно удвоенному отношению площади нормального сечения поры к ее периметру). Макропоры в соответствии с этой классификаций имеют эффективный радиус, превышающий 100,0 нм. Поры, имеющие эффективные радиусы от 100,0 до 15–16 нм, являются переходными. Поры с эффективным радиусом менее 1,5 нм представляют собой микропоры, и к адсорбентам, для которых характерна микропористость, применение понятия удельной поверхности уже необоснован. В дальнейшем, однако, пришлось более детально рассмотреть свойства структур адсорбентов, эффективный радиус пор которых менее 1,5 нм. Де-Бур выделил из общего количества пор с радиусом менее 1,5 – 1,6 нм группу субмикропор радиусом ≤ 0,7 нм. В плоскости сечения таких пор может разместиться не более двух молекул (имеются в виду молекулы азота или аргона - веществ, обычно используемых для измерения адсорбционных характеристик). Способ заполнения таких пор адсорбатом почти не исследован, и к этим порам представления об адсорбирующей поверхности неприменимо. Де-Бур и Ван-дер-Пласс считали, что для пор, имеющих эффективный радиус более 0,7 нм, применение понятия удельной поверхности столь же обосновано, как и для более крупных. В пользу такого представления говорят и расчеты О. Кадлеца, который нашел, что характеристическая энергия адсорбции практически не зависит от радиуса пор в том случае, если ![]() нм и резко возрастает в области
нм и резко возрастает в области ![]() нм.
нм.
В связи с этим возникает необходимость введения еще одной промежуточной классификационной группы, включающей адсорбенты с порами, радиус которых менее 1,5 нм, но больше 0,5 – 0,7 нм. Эти поры получили название супермикропор. Супермикропоры представляют собой переходную область пористости, на протяжении которой характерные черты микропор вырождаются, а свойства мезопор проявляются. Общая удельная поверхность макропор не превышает (2 – 4)·103 м2/кг, а удельная поверхность переходных пор с ![]() нм не превышает 400 – 103 м2/кг.
нм не превышает 400 – 103 м2/кг.
При сравнении экспериментальных величин максимальной адсорбции многих веществ из паров и, особенно, из растворов с максимальными величинами адсорбции, вычисленными для этих значений удельной поверхности по абсолютным изотермам, видно, что большая часть адсорбированного вещества приходится обычно на ту долю пор, которые имеют радиус < 1,5 нм. Однако, рассматривая адсорбцию органических соединений, следует иметь в виду, что поры с радиусом менее 0,5 нм практически недоступны. Следовательно, в области пор с радиусом более 0,5 нм и менее 1,5 — 1,6 нм и осуществляется в основном как адсорбция паров, так и (еще в большей мере) адсорбция из растворов.
При использовании пористых адсорбентов для адсорбции растворенных органических веществ роль отдельных параметров пористой структуры может не соответствовать роли этих параметров при адсорбции паров.
Пористую структуру адсорбентов, применяемых для адсорбции из растворов, целесообразно характеризовать по величинам предельной адсорбции растворенных веществ. Для характеристики удельной поверхности непористых адсорбентов или предельно-адсорбционного объема пористых адсорбентов необходимо определить предельно адсорбированное количество вещества, которое соответствует относительной равновесной концентрации ![]() (С – равновесная концентрация; СS – растворимость). Одним из методов ее вычисления является графический. Метод основан на использовании уравнении теории объемного заполнения микропор.
(С – равновесная концентрация; СS – растворимость). Одним из методов ее вычисления является графический. Метод основан на использовании уравнении теории объемного заполнения микропор.
Теория адсорбции в микропорах была развита М.М. Дубининым. В основу теории положено представление о температурной инвариантности характеристического уравнения адсорбции, выражающего распределение степени заполнения объема адсорбционного пространства микропор по дифференциальной молярной работе адсорбции. Это уравнение имеет следующий вид:
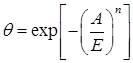
где ![]() – уменьшение свободной энергии,
– уменьшение свободной энергии, ![]() – параметр функции распределения – характеристическая энергия адсорбции,
– параметр функции распределения – характеристическая энергия адсорбции, ![]() – степень заполнения адсорбционной фазы;
– степень заполнения адсорбционной фазы; ![]() – целое число, преимущественно 1, 2, 3.
– целое число, преимущественно 1, 2, 3.
