Основы химии
Сущность и механизм гомогенного катализа.
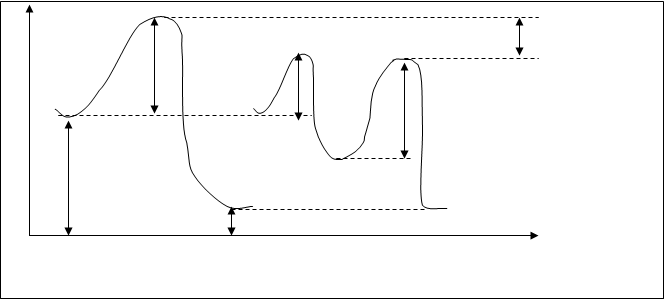 Исходные вещества (реагенты) превращаясь в продукты реакции должны преодолеть энергетический барьер, равный энергии активизации. Еа (рис.10.6.)
Исходные вещества (реагенты) превращаясь в продукты реакции должны преодолеть энергетический барьер, равный энергии активизации. Еа (рис.10.6.)
Н А…В
ΔЕкат.
Еа А…К АК…В
Еа1 Еа2
А+В А+В
К(kat)
AK
ΣН исх. реаг.
АВ АВ+К
ΣН кон.прод.
Путь реакции
Рис.10.6. Энергетическая диаграма а) реакции А+В=АВ без катализатора;
б) каталитической реакции А+В+К=АВ+К
Еа – энергия активации реакции без катализатора;
Еа1 и Еа2 – энергия реакции каталитической реакции;
АК – соединение вещества катализатора с одним из реагентов;
А…К, АК…В – активированные комплексы каталитической реакции;
А…В – активированный комплекс обычной (некатализируемой) реакции;
ΔЕкат. – снижение энергии активизации под действием катализатора.
Сущность гомогенного катализа заключается в том, что катализаторы уменьшают величину энергетического барьера. Это происходит по следующему механизму: катализатор взаимодействует с одним из реагентов, образуя промежуточный комплекс. Затем этот промежуточный (активированный) комплекс взаимодействует с вторым реагентом, образуя конечные продукты и высвобождая катализатор в неизменном первоначальном виде.
За счет образования промежуточного комплекса реагент-катализатор энергтический барьер уменьшается на величину ΔЕкат Примером гомогенного катализа может служить реакция окисления SO2 в SO3 в нитрозном способе получения серной кислоты.
2SO2+O2+NO(кат.)=2SO3+NO
Без катализатора реакция идет медленно и процесс неэффективный. Катализатор, оксид азота (II), первоначально взаимодействует с кислородом, образуя активированный комплекс NO2.
2NO+O2=2NO2
Затем это промежуточное соединение легко взаимодействует с оксидом серы (IV), окисляя его до SO3 и выделяя в первоначальном виде катализатор.
NO2+SO2=SO3+NO
Применение катализатора NO сопровождается уменьшением энергетического барьера на величину ΔЕкат. и значительно ускоряет реакцию.
10.4. Особенности кинетики гетерогенных реакций.
Гетерогенные реакции – это реакции между химическими реагентами, находящимися в различных агрегатных состояниях. Таких процессов очень много. К ним относятся горение топлив, взаимодействие металлов с кислотами, получение азотной кислоты абсорбцией оксидов азота водой, выщепачивание кислотами руд, обработка нефтепродуктов серной кислотой и др.
Особенностью гетерогенных процессов является то, что взаимодействие между реагентами происходит на границе раздела фаз. На скорость таких реакций влияют как химические так и физические факторы. К последним относятся величина поверхности раздела фаз и быстрота переноса вещества из объема к границе раздела и от нее в объем. Для увеличения поверхности раздела фаз необходимо твердое вещество измельчать и распылять один из двух несмешивающихся жидких реагентов. Следовательно, на скорость гетерогенных реакций влияет степень дисперсности реагента. Так как твердое вещество в результате взаимодействия изменяет только свою массу (концентрация его всегда постоянна), то в кинетическое уравнение закона действующих масс твердое вещество не включается.
Как уже было сказано, химическая реакция в гетерогенных системах протекает на поверхности раздела фаз. Для того, чтобы непрерывно протекала реакция необходима постоянная доставка реагента к поверхности раздела фаз и уноса с нее уже образовавшегося вещества. Как видим, процесс делится на три последовательные стадии: диффузия реагента в зону взаимодействия, химическая реакция, удаление продукта реакции.
В соответствии с теорией диффузии: диффузионный поток тем интенсивнее, чем большн разность между концентрацией реагента в данной точке объема (Со) и в зоне реакции (Ср), больше коэффициент диффузии Д и меньше тощина слоя (δ), через который происходит массопередача. В случае стационарного режима (т.е. режима, при котором за рассматриваемый промежуток времени на реакцию расходуется все вещество, доставленное к поверхности раздела фаз), скорость реакции может быть расчитана по следующему уравнению, связывающему скорость процесса с химическим (К) и диффузионным (Д/δ=β) факторами.
V=(K*β/K+β)*Со
Здесь встречается два случая:
1. Медленно протекает сама химическая реакция. (К мало, “химическое сопротивление” К–1 значительное. Процесс протекает в так называемой кинетической области. Для увеличения скорости необходимо применять теже способы воздействия на реакцию, как в гомогенных системах.
2. Медленным является сам процесс переноса вещества (велико “диффузионное сопротивление” β–1). В этом случае для увеличения скорости применяют перемешивание.
Гетерогенный катализ.
Если взаимодействующие вещества и катализатор находятся в разных фазовых (агрегатных) состояниях, катализ – гетерогенный. В гетерогенных каталитических реакциях катализатором является твердое вещество. Например, платиновый катализатор используется при окислении аммиака, катализаторы на основе меди и золота – при синтезе высокомолекулярных соединений (пластмасс и смолы), цинка и хрома – в производстве метанола, ванадий – при получении серной кислоты и т.д.
В случае гетерогенного катализа взаимодействие между реагентами протекает на поверхности катализатора. Механизм процесса состоит из 5-и стадий.
Первая стадия – диффузия реагентов к катализатору.
Вторая стадия – адсорбция реагентов на поверхности катализатора. (на этой стадии происходят изменения в электронном строении реагентов и снижается энергетический барьер).
Третья стадия – реакция на поверхности катализатора.
Четвертая стадия – десорбция продуктов реакции.
Пятая стадия – диффузия продуктов в объем.
Ускорение процесса при гетерогенном катализе, как и в гомогенном, объясняется образованием активированного комплекса. Для увеличения поверхности катализатора его стараются делать губчатым. На выступающих точках (вершинах) катализатора, называемых активными центрами не только адсорбцируются молекулы реагентов, но и претерпивают изменения, в результате которых облегчается образование конечных продуктов.
Рассмотрим этот процесс на примере синтеза аммиака:
N2+H2=2NH3
После адсорбции азота и водорода на поверхности твердого катализатора происходит разрыв связей между атомами азота в молекуле азота N≡N и между атомами водорода в молекуле водорода Н–Н. На эту операцию затрачивается энергия. Однако каждая разорвавшаяся связь в молекуле азота, так же и в молекуле водорода насыщается за счет образования связи с катализатором. Образуется промежуточный комплекс Kat–N и Kat–H. Происходит выделение энергии, чем частично компенсируется затрата энергии на разрыв связей в молекулах реагентов. На последующем этапе происходит разрыв связей в промежуточных комплексах Kat–N и Kat–H и образование молекул продуктов реакции NH3. При этом выделяется значительная энергия и катализатор высвобождается для дальнейших актов взаимодействия.
