Химические методы определения сахаров
1.2.2. Продукты с содержанием лимонной кислоты более 1,5 % и хлебобулочные изделия. Навеску средней гомогенизированной пробы продукта в количестве 10 .15 г, взвешенную с точностью до 0,0001 г, помещают в центрифужную пробирку и подвергают трижды экстракции 30 см3 гексана, объединяя гексановый слой декантированием. Осадок шпателем переносят в коническую колбу вместимостью 100 см3, тщательно смывая остатки со шпателя и пробирки 75 %-ным раствором этанола. Затем трижды экстрагируют содержимое колбы 75 %-ным раствором этанола, подогревая колбу на водяной бане при 60 °С. Отфильтрованные экстракты объединяют и доводят дистиллированной водой до метки в мерной колбе на 100 см3. В мерную пробирку на 10 см3 вносят 5 см3 экстракта и 0,5 см3 насыщенного раствора уксуснокислого свинца. После выпадения осадка надосадочную жидкость в количестве 1,0 см3 переносят в круглодонную колбу вместимостью 10 .25 см3. Туда же вносят на полиэтиленовой пластинке 2 .5 мг ксилита (с точностью до 0,0001 г) и содержимое колбы упаривают на роторном испарителе при 60 °С под вакуумом, после чего проводят силилирование.
2. Силилирование сахаров.
2.1. Способ с использованием трифторуксусной кислоты. В подготовленную навеску образца приливают 1,0 см3 пиридина (нуклеофильный катализатор), 0,9 см3 гексаметилдисилазана, 0,1 см3 трифторуксусной кислоты (облегчающий алкилирование), плотно закрывают и энергично встряхивают в течение 30 секунд. Вначале наблюдают расслоение жидкости на 2 фазы, при этом нижний слой незначителен. По мере стояния раствора в течение 20 .30 минут это расслоение исчезает и начинает выделяться аммиак, что указывает на успешное протекание реакции силилирования:
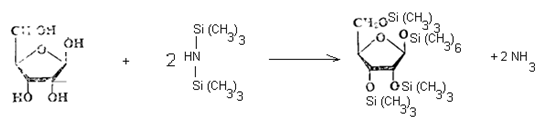
После прекращения выделения аммиака раствор выдерживают 12 часов при комнатной температуре или 1 час при 60 "С. Длительно сохраняющееся расслоение, исчезающее только при нагревании, говорит о том, что реакция силилирования прошла не полностью из-за высокого содержания влаги (более 40%) или повышенного содержания углеводов. В этом случае подготовку пробы повторяют, уменьшив при этом навеску или увеличив время высушивания на роторном испарителе.
![]()
![]() 2.2. Способ с использованием триметилхлорсилана. В подготовленную навеску образца приливают точно 1,0 см3 пиридина, 0,2 см3 гексаметилдисилазана и 0,1 см3 триметилхлорсилана, встряхивают в течение 1 минуты и нагревают в термостате 45 минут при 60 °С:
2.2. Способ с использованием триметилхлорсилана. В подготовленную навеску образца приливают точно 1,0 см3 пиридина, 0,2 см3 гексаметилдисилазана и 0,1 см3 триметилхлорсилана, встряхивают в течение 1 минуты и нагревают в термостате 45 минут при 60 °С:
Затем хроматографируют.
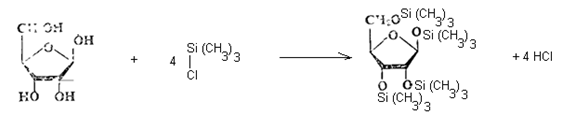
Для упрощения идентификации и количественных расчетов (если не требуется знания аномерного состава сахаров) определение сахаров производят в виде ТМС-производных сахаров. В подготовленную пробу образца добавляют 100 г гидроксиламина солянокислого, приливают 10 см3 пиридина и выдерживают в термостате при 80 °С в течение 2 часов:
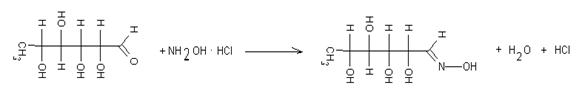
Охлаждают и далее приливают силилирующие агенты.
3. Газохроматографический анализ.
3.1.Подготовка хроматографической колонки. Стеклянную колонку, заполненную готовым сорбентом (количество неподвижной фазы 3 .5% от массы носителя) длиной 2 м и внутренним диаметром З мм устанавливают в термостате хроматографа и проводят термокондиционирование при продувании потоком газа-носителя (гелий, азот, водород) 2 ч при 100°С, 2 ч при 150°С, 4 ч при 200°С и 8 ч при 250"С. Затем устанавливают рабочий режим: температуру колонки профаммируют от 125 до 270°С со скоростью 4 °С в 1 мин, температуру испарителя 250 °С, расход газа-носителя 40см3/мин, температура пламенно-ионизационного детектора 250 °С, продолжают кондиционировать в течение рабочего дня.
3.2.Газохроматографическое определение. 1 мкл пиридинового раствора триметилсилильных производных углеводов вводят в испаритель и элюируют из колонки газом-носителем. Идентификацию индивидуальных триметилсилильных производных проводят по времени удерживания триметилсилильных производных сахаров-метчиков и методом добавок.
3.3. Приготовление стандартных растворов сахаров.
3.3.1. Сахара, имеющие аномеры . Навеску ксилита и навеску определяемого сахара, взятую с точностью 0,0001 г, помещают в коническую колбу и заливают дистиллированной водой до полного растворения углеводов. Раствор выдерживают в течение суток. Аликвотную часть раствора отбирают пипеткой, помещают в круглодонную колбу и упаривают досуха, после чего проводят силилирование.
3.3.2. Сахара, не имеющие аномеров. Силилируются без предварительного растворения.
Массовую долю отдельных сахаров (в %) в навеске продукта определяют по формуле:
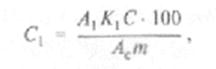
где С, — содержание отдельного сахара в навеске, %; К1 — поправочный коэффициент данного сахара; С — масса навески стандарта, мг; m — масса навески образца; Ас — площадь пика стандарта в относительных единицах; Лс— площадь пика данного сахара в относительных единицах.
Ввиду того, что альфа-лактоза и сахароза выходят на хроматограмме одним пиком, площадь пика альфа-лактозы определяют, исходя из соотношения площадей альфа- и бета-лактозы в модельном соединении лактозы. За основу берется площадь пика бета-лактозы. Площадь пика сахарозы определяют вычитанием от суммарного пика сахарозы пика альфа-лактозы, из пика бета-лактозы. За окончательный результат принимают среднеарифметическое результатов двух параллельных определений и округляют до трехзначной цифры.
Количественное определение сахаров по реакции с пикриновой кислотой (по Крезелиус – Зейферт)
При взаимодействии редуцирующих сахаров с пикриновой кислотой они окисляются до соответствующих кислот, а пикриновая кислота восстанавливается в пикраминовую, обладающую красной или буровато-красной окраской:
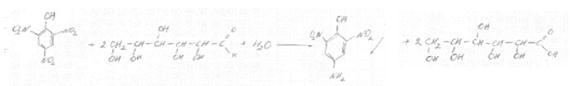
Метод пригоден для количественного определения глюкозы, галактозы, арабинозы, фруктозы, рамнозы, ксилозы, мальтозы, лактозы и крахмала. Метод быстр, но не очень точен. Ошибка может превышать 10-20%. В связи с этим указанный метод имеет ориентировочное значение;
Реактивы и приборы: а) пикриновая кислота, насыщенный раствор; б) углекислый натрий, 20%-ный раствор; в) спектрофотометр.
Ход работы: К 1 мл испытуемого раствора (в котором должно содержаться ее более 3 мг редуцирующих сахаров) прибавляют 2 мл насыщенного водного раствора пикриновой кислоты и 1 мл раствора углекислого натрия, после чего пробирку переносят на 30 мин. в кипящую водяную баню. Охлаждают до комнатной температуры и доводят дистиллированной водой до объема 10 мл. Оптическую плотность раствора определяют при 455 нм (синий светофильтр). Содержание редуцирующих сахаров рассчитывают по калибровочной кривой, составленной по стандартным растворам глюкозы как в работе «Количественное определение сахаров по антроновому методу».
