Общая и неорганическая химия
Каталитические окислительно-восстановительные реакции (ОВР) играют важную роль в промышленности, например:
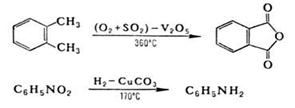
окислительно-восстановительные реакции (ОВР) широко распространены в природе и используются в технике. В основе жизни лежат окислительно-восстановительные реакции (ОВР), происходящие при фотосинтезе, дыхании, транспорте электронов; они же обеспечивают основную часть энергопотребления человечества за счет сжигания органического топлива. Получение металлов, извлечение энергии взрыва основано на окислительно-восстановительных реакциях.
Классификация окислительно-восстановительных реакций
Реакции межмолекулярного окисления-восстановления – это реакции, в которых атом-окислитель и атом-восстановитель принадлежат разным веществам. Эти вещества могут быть как простыми, так и сложными.
4N3-H3 + 3O02 ® 2N02 + 6H2O2-
![]() 2N3- - 6e ® N02 2 восстановитель
2N3- - 6e ® N02 2 восстановитель
O02 + 4e ® 2O2- 3 окислитель
Реакции внутримолекулярного окисления-восстановления – это реакции, в которых атом-окислитель и атом-восстановитель входят в состав одной и той же молекулы или одного и того же иона.
Например, разложение хлората калия
![]() 2KCl5+O2-3 ® 2KCl- + 3O02
2KCl5+O2-3 ® 2KCl- + 3O02
Cl5+ + 6e ® Cl- 2 окислитель
2O2- -4e ® O02 3 восстановитель
Реакции диспропорционирования (самоокисление– самовосстановление) - это реакции, в которых функцию окислителя и восстановителя выполняет один и тот же атом молекулы или иона, находящийся в промежуточной степени окисления. Например:
![]()
![]() 4KCl5+O3 ® 3 KCl7+O4 + KCl-
4KCl5+O3 ® 3 KCl7+O4 + KCl-
Cl5+ - 2e ® Cl7+ 6 3 восстановитель
Cl5+ +6e ® Cl- 2 1 окислитель
Реакции конмутации – реакции внутримолекулярного окисления- восстановления, в результате которых происходит выравнивание степеней окисления атомов одного и того же элемента. Например:
N3-H4N5+O3 = N21+O + 2H2O
Влияние среды на протекание окислительно-восстановительных реакций
Реакции окисления-восстановления могут протекать в различных средах (кислой, нейтральной и щелочной), при этом в зависимости от среды может изменяться характер протекания реакции между одними и теми же веществами. Рассмотрим взаимодействие перманганата калия с сульфитом калия в различных средах.
а) Кислая среда:
2KMn7+O4 + 5K2S4+O3 + 3H2SO4 ® 2Mn2+SO4 + 6K2S6+O4 + 3H2O
![]() Mn7+ + 5e ® Mn2+ 2
Mn7+ + 5e ® Mn2+ 2
S4+ - 2e ® S6+ 5
б) Нейтральная среда:
2KMn7+O4 + 3K2S4+O3 + H2O ® 2Mn4+O2 + 3K2S6+O4 + 2KOH
![]() Mn7+ + 3e ® Mn4+ 2
Mn7+ + 3e ® Mn4+ 2
S4+ - 2e ® S6+ 3
в) Щелочная среда:
2KMn7+O4 + K2S4+O3 + 2KOH ® K2Mn6+O4 + 2K2S6+O4 +H2O
![]() Mn7+ + e ® Mn6+ 2
Mn7+ + e ® Mn6+ 2
S4+ - 2e ® S6+ 1
Схематически это можно представить следующим образом:
Окисленная Восстановленная форма
Форма
![]()
![]() Mn2+ - бесцветный
Mn2+ - бесцветный
![]() Mn7+ ® MnО2 - бурый осадок
Mn7+ ® MnО2 - бурый осадок
![]() MnО42- - зеленый
MnО42- - зеленый
Особые случаи составления уравнений окислительно-восстановительных реакций
Рассмотренная методика составления окислительно-восстановительных реакций применима к большинству простых и сложных процессов. Но в некоторых специальных случаях необходимы дополнительные пояснения.
1. Если число электронов, отдаваемое восстановителем, и число электронов, присоединяемое окислителем, имеют общий наибольший делитель, то при нахождении коэффициентов оба числа делят на него. Например, в реакции
HCl7+O4 + 4S4+O2 + 4H2O = 4H2S6+O4 + HCl1-
основными коэффициентами для восстановителя и окислителя будут не 6 и 2, а 4 и 1.
Если число участвующих в реакции электронов нечетно, а в результате получается четное число атомов, то коэффициенты удваиваются. Например, в реакции
2Fe3+Cl3 + 2HJ1- = J20 + 2Fe2+Cl2 + 2HCl
основными коэффициентами будут не 1 и 1, а 2 и 2.
2. Окислитель или восстановитель иногда дополнительно расходуется на связывание получающихся продуктов (солеобразование).Например, в реакции
Cu + 2HNO3 + 6HNO3 = 3Cu(NO3)2 + 2NO + 4H2O
на окисление на связывание на 3 атома восстановителя Сu0 требуется для окисления 2 молекулы окислителя HNO3; кроме того, на образование нитрата меди - трех молекул - требуется еще 6 молекул HNO3 для связывания трех атомов меди. Таким образом, общий расход азотной кислоты: 2 молекулы на окисление плюс 6 молекул на связывание (солеобразование), то есть всего 8 молекул HNO3. И окончательно уравнение примет вид:
3Cu + 8HNO3 = 3Cu(NO3)2 + 2NO + 4H2O.
З. Если в реакции число элементов, изменяющих свою степень окисления, больше двух, то устанавливают общее число электронов, отдаваемых восстановителями, и общее число электронов, присоединяемых окислителями, а в остальном соблюдается общий порядок составления уравнения реакции. Например,
3As3+2S2-3 + 28HN5+O3 + 4H2O ® 6H3As5+O4 + 9H2S6+O4 + 28N2+O
![]()
![]() 2As3+ - 4e ® 2As5+ -28e 3
2As3+ - 4e ® 2As5+ -28e 3
![]() 3S2- - 24 ® 3S6+
3S2- - 24 ® 3S6+
N5+ + 3e ® N2+ +3e 28
4. Оба элемента – и окислитель, и восстановитель – находятся в одной и той же молекуле. Это реакция внутримолекулярного окисления-восстановления и реакции диспропорционирования. Для удобства подбора коэффициентов в этом случае иногда можно рассматривать процесс как бы идущим справа налево. Например,
3HN3+O2 ® HN5+O3 + 2 N2+O + H2O
![]() N3+ + e ® N2+ 2
N3+ + e ® N2+ 2
N3+ - 2e ® N5+ 1
Продукты окислительно-восстановительных реакций устанавливаются опытным путём

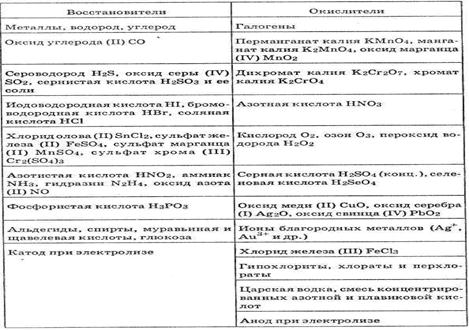
Элементы, имеющие высшую степень окисления, могут быть только окислителями.
Элементы, имеющие низшую степень окисления, могут быть только восстановителями.
Элементы, находящиеся в промежуточной степени окисления, могут и окисляться, и
восстанавливаться, то есть проявляют окислительно-восстановительную двойственностьТипичные окислители: металлы, соединения неметаллов в низшей степени окисленияТипичные восстановители: галогены, О2, N2, вещества, содержащие элемент в высшейСО.
Реакции окисления - восстановления могут протекать в различных средах: в кислой, нейтральной и щелочной. В зависимости от среды может изменяться характер протекания реакции между одними и теми же веществами. Среда влияет на изменение степеней окисления. Рассмотрим пример влияния среды на восстановление перманганат- иона MnO4
