Вода
Вязкость D2O линейно растет с Т до -10ºС. Сдвиговая вязкость в рассматриваемом интервале температур также линейно растет с ростом Т примерно с тем же тангенсом угла наклона. Это означает, что объемная вязкость в этом интервале температур растет, по крайней мере пропорционально квадрату температуры в D2O.
Скорость звука
Скорость звука в легкой и тяжелой воде и эквимолярной смеси начинает уменьшаться при Т = 40ºС. При 50ºС она равна 1550 м/с в Н2О, 1500 м/с в смеси Н2О и D2O и 1450 м/с в D2O. При -10ºС скорость звука в Н2О равна •1350 м/с. В смеси Н2О и D2O •1300 м/с и в D2O•1250 м/с. Так как плотность воды в этом интервале температур изменяется мало, то уменьшение скорости звука определяется увеличением адиабатической сжимаемости.
Таким образом, из представленных выше данных следует, что Н и D неэквивалентны в воде. Этот вывод следует:
1. Из различной зависимости разности давлений пара над переохлажденной водой и льдом от температуры Н2О и D2O (Краус, Грир, 1984). Поведение ![]() и
и ![]() после достижения максимума, различно. Так, в D2О давление пара над жидкостью оказывается большим, чем это следует из теории, а в Н2О наоборот.
после достижения максимума, различно. Так, в D2О давление пара над жидкостью оказывается большим, чем это следует из теории, а в Н2О наоборот.
2. Замена Н на D, по данным Доре, очень сильно зависит от их концентрации. Добавление D2O в Н2О трансформирует ![]() , уширяет максимум, расположенный на расстоянии 3,4 Å.
, уширяет максимум, расположенный на расстоянии 3,4 Å.
3. С увеличением давления в воде от 0 до 5000 бар ширина линии ОН распределения (Габалла, Нельсон, 1983) монотонно уменьшается. Ширина линии OD растет с ростом давления и имеет максимум при давлении 2000-3000 бар.
4. Время спин-решеточной релаксации в Н2О монотонно уменьшается с ростом давления вплоть до 9000 бар (Джонос, 1976). В D2O при давлениях 2000-7000 бар время спин-решеточной релаксации имеет максимум.
5. Коэффициент самодиффузии молекул в D2O имеет максимум в районе 2000-3000 бар при температурах, близких к 0ºС.
Эти факты, на наш взгляд, свидетельствуют в пользу того, что силы молекулярного взаимодействия в Н2О и D2O различно зависят от Т и Р.
Согласно Цунделю, энергия дисперсионного взаимодействия туннелирующих протонов определяется следующим выражением:
 ,
,
где 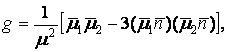
![]() - частота протонных переходов,
- частота протонных переходов, ![]() -время релаксации системы после нарушения равновесия и
-время релаксации системы после нарушения равновесия и ![]() и
и ![]() - диэлектрические постоянные воды,
- диэлектрические постоянные воды, ![]() - дипольный момент перехода протона. Представленное выражение свидетельствует в пользу того, что дисперсионное взаимодействие в Н2О больше, чем D2О, так как
- дипольный момент перехода протона. Представленное выражение свидетельствует в пользу того, что дисперсионное взаимодействие в Н2О больше, чем D2О, так как ![]() .
.
Смещение максимума плотности в D2O в область более высоких температур, чем в Н2О, обусловлено тем, что в D2О сильнее локальное взаимодействие и слабее дисперсионное.
Более детальное исследование зависимостей дисперсионного взаимодействия от Т и Р в Н2О и D2О позволит теоретически описать неэквивалентность Н и D и объяснить аномалии изотопных эффектов D2O.
Растворяющая способность тяжелой воды меньше, чем легкой. Для изотермических реакций количество тепла, выделяемое в процессе реакций в D2O больше, чем в Н2О, а при эндотермических реакциях тепла в результате реакции поглощается больше в D2O, чем в Н2О. Все процессы нейтрализации в тяжелой воде идут быстрее, а все процессы диссоциации в тяжелой воде происходят более медленно. Это связано с тем, что константа скорости рекомбинации больше в тяжелой воде, а постоянная скорости диссоциации больше в легкой воде.
ЗАКЛЮЧЕНИЕ
Молекула Н2О представляет собой уникальный двойной симметричный донор и акцептор протонов. В зависимости от Т и Р в конденсированном состоянии в системе одинаковых молекул Н2О осуществляются синхронные переходы протонов как между молекулами, так и внутри молекул Н2О. Внутри молекул в неоднородном поле соседей протоны переходят от поделенных пар электронов молекулы к неподеленным парам. Между молекулами Н2O протоны переходят от поделенных пар электронов одной молекулы к неподеленным парам электронов других молекул, окружающих данную. Протонные переходы между молекулами обусловливают протонный беспорядок в группе льдов и в жидкой воде. Протонные переходы внутри молекул определяют физические свойства льдов без протонного беспорядка и жидкой воды.
Взаимодействие осциллирующих между молекулами и внутри молекул протонов представляет собой дисперсионное взаимодействие одинаковых осцилляторов. Энергия дисперсионного взаимодействия осциллирующих протонов может быть оценена по формуле Лондона
![]() •
•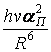 ,
,
где ![]() - частота протонных переходов, равная 1000 см-1 в Н2О и 700 см-1 в D2О;
- частота протонных переходов, равная 1000 см-1 в Н2О и 700 см-1 в D2О; ![]() - протонная поляризуемость
- протонная поляризуемость
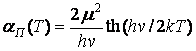 (Цундель, 1971);
(Цундель, 1971);
и по формуле Цунделя
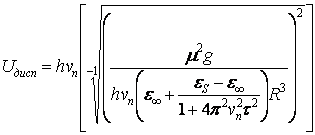 ,
,
где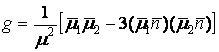 - ориентационная зависимость дипольных моментов переходов протонов.
- ориентационная зависимость дипольных моментов переходов протонов.
Согласно развиваемой гипотезе во льду I с линейными водородными связями, энергия взаимодействия молекул Н2О определяется как локальным взаимодействием соседних молекул, так и дисперсионным взаимодействием осциллирующих между молекулами протонов. Ширина линий в КР спектрах Н2О и спектрах 5% Н2О в D2O и наоборот свидетельствуют в пользу того, что энергия дисперсионного взаимодействия в Н2О больше, чем локального.
Структуру бездефектных льдов и молекулярное взаимодействие в них, на наш взгляд, полностью определяет дисперсионное взаимодействие осциллирующих внутри молекул Н2О протонов в искаженном внешним давлением электрическом поле соседних молекул. Расстояния между ближайшими соседями в структуре льда VIII, которые не связаны водородными связями, короче, чем между водородосвязанными молекулами.
Неэквивалентность Н и D является следствием одновременного действия локальных и дисперсионных молекулярных сил взаимодействия, энергия которых по разному зависит от Т и Р в Н2O и D2О.
Области синхронных осцилляций протонов во льдах и жидкой воде велики и протираются до ~10-12 см3, что обусловлено низкой, по сравнению с электронной, частотой осцилляций протонов.
